Nội dung bài viết
Oxit kẽm là một oxit của kẽm, có công thức hóa học ZnO, ở dạng bột mịn màu trắng. Vậy đặc tính độc đáo của Zinc Oxide là gì? Cấu tạo, phương pháp và ứng dụng trong đời sống? Mọi thắc mắc sẽ được giải đáp qua bài viết dưới đây.
1. Kẽm oxit – ZnO là gì?
Kẽm oxit là một hợp chất kẽm, được hình thành bởi liên kết giữa các nguyên tử kẽm và oxy, có công thức hóa học ZnO.
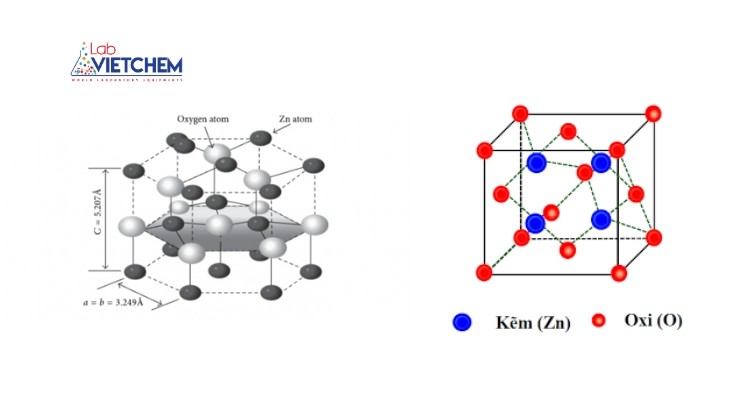
Cấu trúc oxit kẽm
Nó tồn tại dưới dạng bột màu trắng, có vai trò quan trọng trong sản xuất và đời sống.
Tên gọi khác: Kẽm trắng, Calamine, len triết gia, trắng Trung Quốc, kẽm hoa,… Trong đó, kẽm trắng là thuật ngữ dùng để chỉ ZnO được tổng hợp từ phương pháp đốt kim loại kẽm.
2. Quá trình hình thành ZnO
Từ xa xưa, con người đã biết ZnO là sản phẩm phụ của quá trình nấu chảy đồng. Người La Mã sử dụng nó để luyện đồng thau và làm thuốc mỡ.
Vào giữa thế kỷ 18, nhà hóa học người Đức Cramer đã khám phá ra cách đốt kẽm kim loại để thu được ZnO. Nhưng phải đến năm 1840, người ta mới áp dụng rộng rãi phương pháp này để điều chế oxit kẽm thay thế chì trắng. Bởi ưu điểm của ZnO là không độc hại và không bị đen trong môi trường không khí.
3. Tính chất đặc trưng của ZnO
3.1. Tính chất vật lý
– Ngoại quan: Tồn tại dưới dạng bột màu trắng, mịn, nhưng khi đun nóng trên 300 độ C thì chuyển sang màu vàng, khi để nguội lại chuyển sang màu trắng.

Bột oxit kẽm
– Hấp thụ tia cực tím và ánh sáng có bước sóng < 366 nm.
– Khối lượng phân tử là 81,3984 g/mol
– Mật độ là 5,606 g/cm3
– Nhiệt độ nóng chảy: 1975°C tương ứng với 2248 K hoặc 3587°F.
– Nhiệt độ sôi: 2360°C tương ứng với 2630 K hoặc 4280°F.
– Độ hòa tan trong nước ở 30 độ C là 0,16 mg/100 mL.
3.2. Tính chất hóa học
– Oxit kẽm có tính chất của oxit lưỡng tính. Hiệu quả với hầu hết các axit như HCl, H2SO4, HNO3,…
ZnO + 2 HCl → ZnCl2 + H2O
– Phản ứng với dung dịch bazơ với muối phức tạo thành sản phẩm theo phương trình sau:
ZnO + 2NaOH + H2O → Na2(Zn(OH 4))
– Nó cũng phản ứng chậm với các axit béo trong dầu để tạo ra các carboxylat tương ứng, ví dụ như oleate hoặc stearat.
– Phản ứng phân hủy tạo thành sản phẩm là hơi kẽm và oxy.
ZnO + C → Zn + CO
– Phản ứng với hydro sunfua: Sản phẩm tạo thành là kẽm sunfua.
ZnO + H2S → ZnS + H2O
4. Tóm tắt các phương pháp điều chế ZnO
4.1. Phương pháp gián tiếp
Áp dụng 2 giai đoạn bao gồm nhiệt phân và oxy hóa. Đây là phương pháp được sử dụng phổ biến trong sản xuất oxit kẽm với quy trình sau:
– Bước 1: Đun chảy kẽm kim loại nguyên chất trong nồi nấu bằng than chì.
– Bước 2: Ở nhiệt độ trên 90 độ C, hơi kẽm sẽ bốc lên và bị oxy hóa trong không khí tạo thành oxit kẽm.
– Bước 3: Cung cấp nguồn ánh sáng rực rỡ cùng với việc giảm nhiệt độ là điều kiện cần để tạo ra các hạt oxit kẽm.
– Bước 4: Qua ống truyền nguội ta thu được các hạt oxit kẽm. 4.2. Phương pháp trực tiếp
ZnO có thể được điều chế trực tiếp bằng cách sử dụng các hợp chất chứa kẽm không tinh khiết như calamine hoặc kẽm kim loại làm đầu vào cho quá trình tổng hợp oxit kẽm.
Đun nóng vật liệu này và khử cacbon để tạo thành hơi kẽm và hơi nước. Trải qua quá trình oxy hóa gián tiếp để tạo thành oxit kẽm.
4.3. Chuẩn bị trong phòng thí nghiệm
Ở quy mô phòng thí nghiệm, oxit kẽm được sản xuất bằng phương pháp điện phân anốt dung dịch NaHCO3 bằng thanh kẽm. Phương pháp này sẽ tạo ra kẽm hydroxit và hydro.
Sản phẩm tạo thành là kẽm hydroxit, chất này bị thủy phân để tạo thành oxit kẽm bằng cách nấu chảy.
Zn + 2 H2O → Zn (OH) 2 + H2
Zn(OH)2 → ZnO + H2O
5. Vai trò của oxit kẽm trong nhiều lĩnh vực của đời sống
5.1. Sản xuất cao su
Trong ngành sản xuất cao su, có tới 50% ZnO được sử dụng. Nó kết hợp với axit stearic được sử dụng trong quá trình lưu hóa cao su. Bên cạnh đó, nó còn giúp bảo vệ cao su khỏi nấm mốc và tia UV.

Oxit kẽm tạo ra cao su
5.2. Ngành xây dựng
Đây là nguyên liệu dùng để sản xuất bê tông, giúp tăng thời gian đông kết và khả năng chống nước của bê tông.
5.3. Thuốc thẩm mỹ
Nó là một thành phần trong công thức thuốc mỡ và kem chống nắng giúp bảo vệ da tay khỏi các tác nhân gây hại như tia UV.
ZnO có trong thuốc mỡ
ZnO được thêm vào dầu gội trị gàu và nấm da đầu, phấn rôm trẻ em để hạn chế rôm sảy ở trẻ em.
5.4. lĩnh vực y tế
ZnO là một thành phần trong kem và thuốc mỡ để:
– Trị viêm da, chàm,…
– Điều trị da khô, các bệnh về da và nhiễm trùng da như da bị kích ứng, tổn thương.
– Se khít nông, không để vết bỏng lớn.
– Tình trạng da bị cháy nắng và bệnh rosacea.
5.5. Ngành sơn
ZnO đóng vai trò là chất tạo màu trong sơn, đặc biệt được sử dụng trong sơn cho giấy. Ngoài ra còn tạo lớp phủ chống ăn mòn trên kim loại, đặc biệt là sắt mạ kẽm.
5.6. Các ngành công nghiệp khác
– Có tác dụng khử mùi, kháng khuẩn do có khả năng thấm hút chất lỏng nên thường được bổ sung vào các chất liệu khác như bông, cao su, bao bì thực phẩm.
– Được tìm thấy trong đầu lọc thuốc lá để loại bỏ một số thành phần khỏi khói thuốc lá.
– Đóng vai trò là chất phụ gia trong nhiều sản phẩm.
– ZnO nghèo trong đồng vị kẽm có khối lượng nguyên tử 64 dùng để chống ăn mòn trong lò phản ứng hạt nhân nước áp lực.
>> Xem thêm: Kẽm là nguyên tố gì? Vai trò trong cuộc sống
6. Kẽm oxit – ZnO có độc không?
Khi sử dụng với lượng khuyến nghị, ZnO được coi là an toàn, nhưng nếu sử dụng ở nồng độ cao, nó có thể gây ra những ảnh hưởng tiêu cực đến sức khỏe, cụ thể:
– Zinc Oxide trong kem chống nắng có nguy cơ cao khiến ZnO-NP hấp thụ vào máu và gây độc.
– Hạt nano ZnO trong thực phẩm đóng hộp có thể tích tụ trong tế bào ở đường tiêu hóa và gây ra sự thay đổi hoặc mất đi lớp bảo vệ thành ruột. Điều này sẽ làm giảm khả năng hấp thụ chất dinh dưỡng của cơ thể.
– Ngoài ra, hạt nano ZnO có thể làm tăng tính thấm của mô ruột, tạo điều kiện thuận lợi cho các hợp chất có hại xâm nhập vào ruột và đi vào dòng máu.
Trên đây là những chia sẻ về hóa chất ZnO với bạn đọc. Nếu bạn có bất kỳ thông tin hoặc thắc mắc nào, vui lòng liên hệ với chúng tôi để được giải đáp qua website labvietchem.com.vn hoặc số điện thoại nóng 0826 020 020 để được tư vấn nhanh nhất.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn