Nội dung bài viết
SiO2 là chất có rất nhiều ứng dụng trong cuộc sống như làm kính cửa sổ, lọ thủy tinh,… Vậy có bao giờ bạn thắc mắc? SiO2 là gƠ? Tính chất hóa học của nó là gì, nó được điều chế và ứng dụng như thế nào? Nếu vậy thì hãy cùng LabvietCHEM đi tìm câu trả lời qua bài viết dưới đây nhé.

SiO2 SiO2 là gì?
SiO2 là gì?
SiO2 hay silicon dioxide là một hợp chất hóa học còn được gọi là silica. Nó là một oxit silic có độ cứng cao được biết đến từ thời cổ đại. Các phân tử SiO2 không tồn tại ở dạng đơn lẻ mà liên kết với nhau tạo thành các phân tử rất lớn và tồn tại ở hai dạng: tinh thể và vô định hình. Hầu hết silicon dioxide được tổng hợp nhân tạo được tạo ra ở dạng bột hoặc dạng keo và có cấu trúc vô định hình, nhưng nếu được tạo ra ở áp suất và nhiệt độ cao như coesite và stishovite, nó có cấu trúc tinh thể.
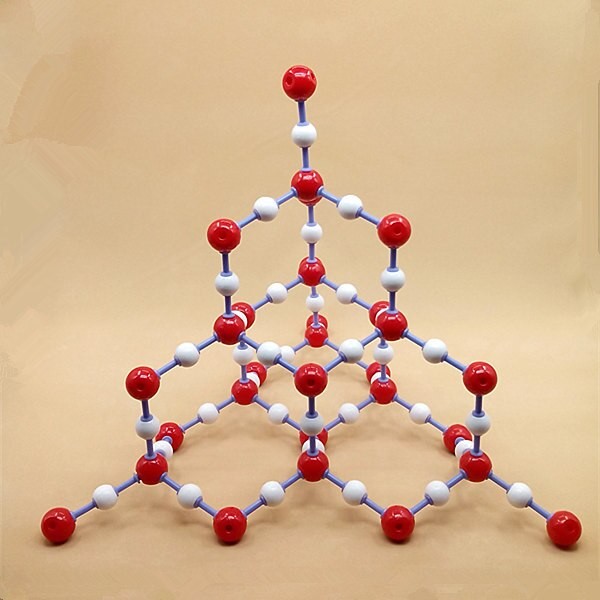
Cấu trúc tinh thể SiO2
Trạng thái tự nhiên của silicon dioxide SiO2
Trong tự nhiên, silicon dioxide tồn tại chủ yếu ở dạng tinh thể hoặc vi tinh thể như cát (thạch anh), tridimite, cristobalite, cancedoan hoặc mã não, trong đó dạng phổ biến nhất là cát. Nó là một khoáng chất của vỏ Trái đất.

Tinh thể thạch anh SiO2
Trong điều kiện áp suất bình thường, silicon dioxide tinh thể có ba dạng thù hình chính: thạch anh, tridimite và cristobalite. Mỗi dạng có hai hoặc ba dạng thứ cấp với dạng thứ cấp α ổn định ở nhiệt độ thấp và dạng thứ cấp β ổn định ở nhiệt độ cao.
Ba dạng tinh thể của SiO2 có sự sắp xếp khác nhau của các nhóm tứ diện SiO4 trong tinh thể. Ở dạng thạch anh α, góc liên kết Si-O-Si là 150°, còn ở dạng tridimite và cristobalite, góc liên kết Si-O-Si là 180°. Trong thạch anh, các nhóm tứ diện SiO4 được sắp xếp sao cho các nguyên tử Si nằm theo đường xoắn ốc quay phải (α-thạch anh) hoặc quay trái (β-thạch anh). Để biến thạch anh thành cristobalite, góc Si-O-Si cần thay đổi từ 150° thành 180°. Nếu muốn biến nó thành α-tridimite, ngoài việc thay đổi góc Si-O-Si từ 150° thành 180°, bạn còn phải xoay tứ diện SiO4 quanh trục đối xứng 180°.
Tính chất hóa học của SiO2
– Silicon dioxide có thể phản ứng với chất kiềm và oxit bazơ tạo thành muối silicat ở nhiệt độ cao
SiO2 + 2NaOH → Na2SiO3 + H2O
SiO2 + Na2CO3 → Na2SiO3 + CO2
– Không phản ứng với nước.
– Phản ứng với axit flohydric theo phương trình hóa học:
SiO2 + 4HF → SiF4 + 2H2O
SiO2 + 6HF(ngưng tụ) → H2SiF6 + 2H2O
Phương pháp điều chế SiO2
Mặc dù silicon dioxide rất phổ biến trong tự nhiên nhưng chúng ta cũng có thể tổng hợp nó bằng một trong các phương pháp sau:
- Để silicon phản ứng với oxy ở điều kiện nhiệt độ cao
Si(r) + O2(k) → SiO2 (r)
Phương pháp này thường được sử dụng để phủ lớp SiO2 lên bề mặt silicon.
- Phương pháp phun khói
Đó là phương pháp thủy phân halogen gel ở nhiệt độ cao bằng oxy và hydro theo phương trình hóa học:
2H2 + O2 + SiCl4 → SiO2 + 4HCl
- Phương pháp lượng mưa
Cho silic lỏng phản ứng với axit vô cơ. Phản ứng xảy ra như sau:
Na2SiO3 + H+ → 2Na+ + SiO2 + H2O
- Phương pháp Sol-gel
Phương pháp thủy phân alkoxysilane bằng chất xúc tác bazơ hoặc axit. Phương trình phản ứng như sau:
Si(OR)4 + 2H2O → SiO2 + 4ROH
Ngoài ra, silica NanospringsTM được sản xuất bằng phương pháp hơi lỏng-rắn ở nhiệt độ thấp, tương đương với nhiệt độ phòng.
Ứng dụng của silicon dioxide SiO2
– Khoảng 95% silicon dioxide thương mại được sử dụng trong ngành xây dựng, ví dụ như trong sản xuất bê tông. Hỗn hợp đá vôi và đất sét sau khi được nghiền nhỏ sẽ được trộn với cát và nước tạo thành bùn. Sau đó nung ở nhiệt độ khoảng 1400 – 1500°C trong lò nung xi măng (lò quay hoặc lò đứng) để tạo ra clinker rắn, sau đó để nguội. Nghiền clinker và một số chất phụ gia thành dạng bột, chúng ta sẽ thu được xi măng.

Là nguyên liệu sản xuất xi măng
– Là nguyên liệu trong ngành sản xuất gốm sứ: Trộn đất sét, thạch anh và fenspat với nước theo tỷ lệ thích hợp để tạo thành khối dẻo rồi tạo hình. Sau đó, nướng các đồ vật có hình dạng ở nhiệt độ thích hợp.

Là nguyên liệu trong ngành sản xuất gốm sứ
– Là nguyên liệu quan trọng để sản xuất thủy tinh: Trộn đều hỗn hợp cát, đá vôi, soda theo tỷ lệ thích hợp, sau đó nung trong lò quay ở nhiệt độ 900°C để tạo thành bột thủy tinh. Tiếp theo là làm nguội phần thủy tinh nhão để có được loại thủy tinh dẻo. Và công đoạn cuối cùng là ép hoặc thổi tấm kính dẻo thành những hình dạng mong muốn.
CaCO3 (t°) → CaO + CO2
CaO + SiO2 (t°) → CaSiO3
Na2CO3 + SiO2 (t°) → Na2SiO3 + CO2

Sản xuất thủy tinh từ cát thạch anh
– Thạch anh được sử dụng trong hệ thống lọc nước và xử lý nước tinh khiết.
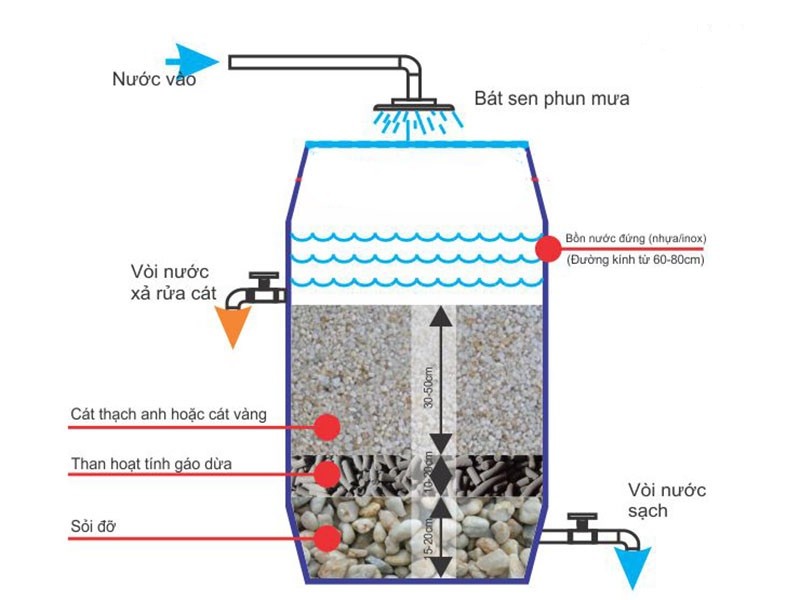
Hệ thống lọc nước sử dụng silicon dioxide
– Sản xuất Natri silicat (Na2SiO3) – nguyên liệu làm xà phòng và thuốc nhuộm.
– SiO2 ở dạng cát được sử dụng làm thành phần chính trong quá trình đúc cát để sản xuất các chi tiết, đồ vật bằng kim loại vì có nhiệt độ nóng chảy cao.
Đó là một số thông tin về silicon dioxide SiO2 là gì? mà LabTrường Lê Hồng Phong đã biên soạn. Chắc chắn sau khi theo dõi nội dung trên thì bạn đã giải đáp được những thắc mắc ban đầu rồi phải không? Hãy truy cập ngay website labvietchem.com.vn để xem thêm nhiều bài viết hay và hữu ích.
Xem thêm:
- Ethylene là gì? Cơ chế làm chín quả bằng ethylene C2H4
- Propylene Glycol – Tính chất, phương pháp sản xuất và ứng dụng trong đời sống


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn