Nội dung bài viết
Có thể bạn chưa biết Kali là gì nhưng chắc chắn hầu hết chúng ta đều biết đến nguyên tố hóa học Kali. Trên thực tế, Kali và Kali đều là tên của một kim loại mềm trong bảng tuần hoàn. Lab VietChem sẽ giúp bạn hiểu rõ hơn về tính chất lý hóa cũng như những ứng dụng cơ bản của Kali trong bài viết sau đây!
1. Kali là gì?
Kali là tên gọi khác của nguyên tố hóa học Kali, ký hiệu K. Khái quát chung, Kim loại Kali mềm, có màu trắng bạc và có khả năng bị oxy hóa rất nhanh trong môi trường không khí.
Sự tồn tại của nguyên tố Kali là vô cùng cần thiết cho sự sống. Từ cơ thể các sinh vật sống, trong đó có con người, cho đến các hoạt động trong các lĩnh vực công nghiệp, nông nghiệp, thủy sản,… đều cần đến Kali.

nguyên tố Kali
2. Khối lượng nguyên tử và đồng vị của Kali
Khối lượng nguyên tử của Kali là 39,0893, số hiệu nguyên tử là 19. Theo đó, trong 1 nguyên tử Kali có 19 proton và 19 electron, bán kính nguyên tử trung bình khoảng 2,77 Pm, Vm là 45,46 cm³/mol.
Kali là nguyên tố phổ biến thứ bảy trong lớp vỏ Trái đất, chiếm khoảng 2,4% khối lượng của lớp này. Nguyên tố Kali có 3 đồng vị tự nhiên gồm: K39 (93,3%), K40 (0,01%) và K41 (6,7%).
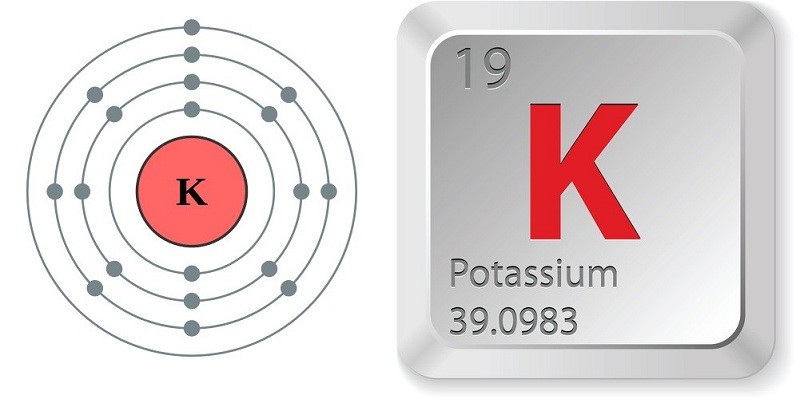
Khối lượng nguyên tử và đồng vị của Kali
3. Tính chất đặc trưng của Kali
Kali là kim loại có nhiều tính chất vật lý và hóa học độc đáo. Bao gồm:
3.1. Tính chất vật lý
Một câu hỏi là, Kali là kim loại hoặc phi kim? Theo đó, kali là kim loại, nhẹ thứ hai chỉ sau nguyên tố Lithium. Trọng lượng riêng của Kali là 0,863 g/cm3.
Mặc dù là kim loại nhưng Kali có thể dễ dàng cắt bằng dao vì nguyên tố này rất mềm. Nhiệt độ nóng chảy chỉ khoảng 63 độ C và nhiệt độ sôi đạt tới 760 độ C.
3.2. Tính chất hóa học
Kali có tính khử rất mạnh. Theo đó, có thể kể đến một số tính chất hóa học đặc trưng của kim loại kiềm này như:
– Tác dụng với phi kim: Kali phản ứng với oxy tạo ra oxit, phản ứng với các phi kim loại khác tạo ra muối và làm cho ngọn lửa có màu hoa cà.
4K + O2 → 2K2O
2K + Cl2 → 2KCl
– Phản ứng với axit loãng: Kali phản ứng với axit loãng tạo ra muối và hydro.
2K + 2HCl → 2KCl + H2
– Tác dụng với nước: K phản ứng với nước tạo ra dung dịch kiềm đồng thời giải phóng khí hydro.
2K + 2H2O → 2KOH + H2.
– Phản ứng với hydro: Trong điều kiện áp suất cao và nhiệt độ cao từ 350 độ C đến 400 độ C, Kali phản ứng với hydro tạo thành Kali hydrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
4. Điều chế Kali như thế nào?
Với công nghệ hiện đại, việc điều chế Kali có thể được thực hiện bằng nhiều cách khác nhau. Theo đó, hiện nay có 3 cách cơ bản để điều chế nguyên tố hóa học đặc biệt này:
4.1. Công nghệ Griesheim
Với công nghệ Griesheim, Kali được tạo ra bằng cách phản ứng giữa hợp chất Kali Fluoride và Canxi Carbide. Phương trình cho phản ứng hóa học này như sau:
2KF + CaC2 → 2K + CaF2 + 2 C
4.2. Điện phân hydroxit
Điện phân hydroxit dưới nhiệt độ cao là quá trình cô lập các nguyên tố trong hợp chất, tạo ra Kali một cách độc lập. Phương trình phản ứng như sau:
4KOH n/c→ 4K + O2 + 2H2O
4.3. Điện phân kali clorua
Điện phân Kali Clorua cũng là phương pháp phổ biến để điều chế Kali với phương trình phản ứng là:
2KCl n/c → 2K + Cl2
5. Vai trò của Kali trong nhiều lĩnh vực
Tầm quan trọng của Kali trong đời sống con người là không hề nhỏ. Một số vai trò cơ bản của Kali bao gồm:
5.1. Đối với con người
Đối với con người, Kali có tác dụng gì?? Đầu tiên, Kali giúp cân bằng lượng nước và khoáng chất được cơ thể hấp thụ và đào thải. Giúp hạn chế nguy cơ mắc các bệnh liên quan đến huyết áp cao, sỏi thận, loãng xương… Đồng thời, hỗ trợ tích cực cho hoạt động cơ bắp trơn tru hơn.
5.2. Đối với lĩnh vực công nghiệp
Lượng tiêu thụ kali hàng năm trong lĩnh vực công nghiệp có thể lên tới hàng triệu tấn. Một số lĩnh vực quan trọng cần có sự góp mặt của Kali bao gồm: Sản xuất thuốc súng, sản xuất thủy tinh, công nghiệp xà phòng và chất tẩy rửa, công nghiệp dệt nhuộm…
Các sản phẩm hàng ngày chúng ta sử dụng có chứa nguyên tố Kali bao gồm: Mực, thuốc nhuộm, đèn huỳnh quang, diêm an toàn, giấy bẫy ruồi…
5.3. Để sản xuất phân bón
Vai trò của Kali trong cơ thể thực vật là rất quan trọng, ảnh hưởng trực tiếp đến sự sinh trưởng và phát triển mọi mặt của cây trồng. Vì vậy, phân bón chứa kali được sử dụng ở dạng hợp chất Kali clorua (KCl), Kali sunfat (K2SO4), Kali natri (KNO3)…

Kali được sử dụng để sản xuất phân bón
5.4. Trong phòng thí nghiệm
Một đặc tính khác của Kali và các hợp chất Kali là khả năng truyền nhiệt tốt. Vì vậy, trong phòng thí nghiệm, hợp kim kali và natri được sử dụng làm môi trường truyền nhiệt.
6. Mức độ an toàn của Kali
Kali – một hoạt chất quan trọng đối với đời sống và sức khỏe con người. Tuy nhiên, nếu chế độ ăn chứa quá ít hoặc quá nhiều nồng độ Kali cũng có thể gây ra những hậu quả tiêu cực.
Nếu nồng độ kali không ở mức tiêu chuẩn có thể dẫn đến yếu cơ, nhịp tim nhanh, chóng mặt, đau đầu và sưng khớp. Nếu không có sự hỗ trợ kịp thời và hồi phục nhanh chóng sẽ gây ảnh hưởng không nhỏ đến tim mạch.

Kali có trong tự nhiên rất dồi dào nhưng cần được bổ sung với liều lượng vừa đủ để tốt cho sức khỏe
7. Mua Kali ở đâu uy tín, chất lượng, giá rẻ?
Lab VietChem là đơn vị chuyên cung cấp các sản phẩm, hóa chất cho ngành công nghiệp. Sự đa dạng của các loại hóa chất thông dụng tại đơn vị đã trở thành một trong những lợi thế lớn của thương hiệu, đáp ứng được nhu cầu của mọi khách hàng.
Đến với LabvietChem khách hàng sẽ được tư vấn và cung cấp các dụng cụ, hóa chất thiết yếu trong nhiều ngành nghề khác nhau. Tận hưởng các chính sách bán hàng, chính sách vận chuyển, chương trình bảo hành và phương thức hỗ trợ thanh toán tối ưu.
LabvietChem vừa chia sẻ một số thông tin về Kali. Hy vọng nội dung bài viết đã phần nào giúp bạn có thêm hiểu biết về nguyên tố hóa học đặc biệt này. Nếu bạn muốn được tư vấn chi tiết hơn về Kali hoặc có nhu cầu mua hóa chất chính hãng, vui lòng liên hệ Labvietchem theo số HOTLINE: 0826.020.020 để được hỗ trợ tận tình, chu đáo.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn