Nội dung bài viết
Cumen được biết đến là nguyên liệu quan trọng dùng để điều chế các chất hữu cơ có nhiều ứng dụng như axeton, phenol, v.v. Vậy cumen là gì? Ngoài những ứng dụng trên, chúng còn được dùng vào việc gì khác không? Hãy cùng Labvietchem theo dõi những thông tin dưới đây để tìm câu trả lời nhé.
1. Tổng quan về cumen là gì?
1.1. Cumen là gì?
Cumen hay isopropylbenzen là một chất dễ cháy, có công thức phân tử C9H12. Nó là một hydrocarbon bao gồm một vòng thơm và một nhóm thế propyl và cũng là một dẫn xuất của benzen.
Tên gọi khác: isopropyl benzen, cumene, cumol,…
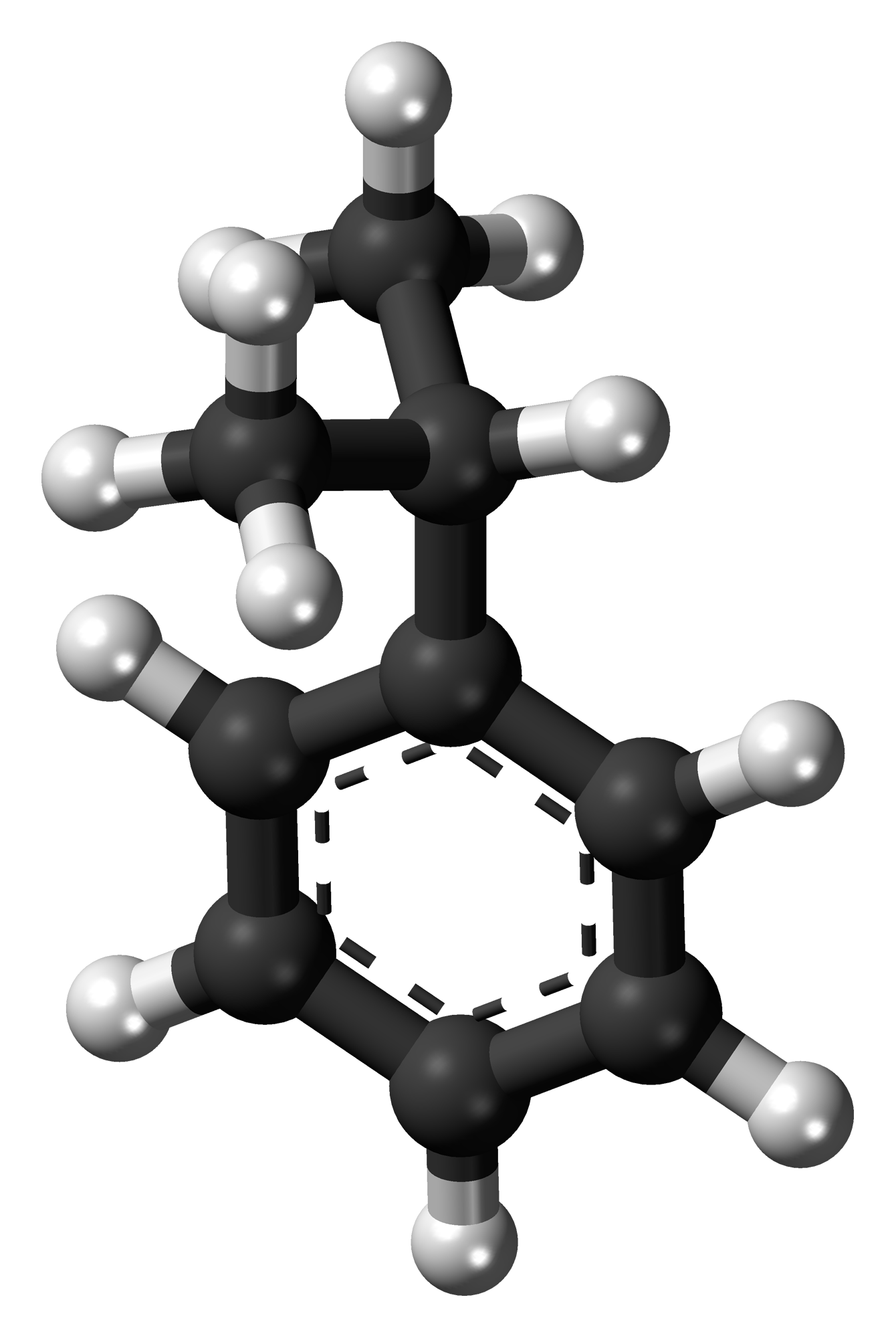
Cumen là gì?
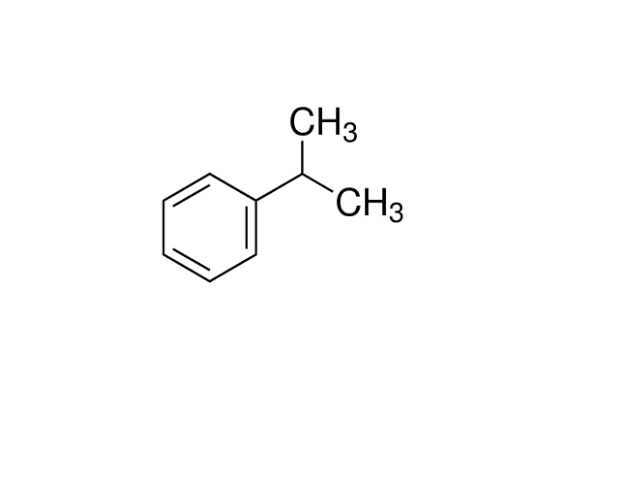
1.2. Công thức cấu tạo của cumen là gì?
Công thức cấu tạo của cumen là C6H5-CH(CH3)-CH3
1.3. Nguồn gốc của cumen là gì?
- Được tạo ra trong quá trình tinh chế hoặc đốt các sản phẩm dầu mỏ
- Từ một số quy trình công nghiệp như: cao su, hóa chất, giấy, nhựa, sơn,…
- Phát ra từ vecni, sơn, khói thuốc lá, v.v.
- Có thể tìm thấy trong khí thải động cơ
- Phát sinh từ một số sản phẩm tiêu dùng như sàn và tấm ốp tường cao su, nhựa cách nhiệt, đồ gỗ nội thất…
2. Tính chất lý hóa nổi bật của cumen
2.1. Tính chất vật lý
|
Kiểm tra bên ngoài |
Chất lỏng không màu |
|
Mùi |
Sáp có mùi như xăng |
|
khối lượng cụ thể |
0,862 g cm-3 |
|
điểm sôi |
152 độ C |
|
điểm nóng chảy |
-98 độ C |
|
Độ hòa tan trong nước |
tầm thường |
|
độ hòa tan |
Độ hòa tan trong axeton, etanol và ete |
|
Tài sản khác |
|
2.2. Tính chất hóa học
Chứa tất cả các tính chất của vòng benzen cùng với gốc alkyl
– Có mặt trong phản ứng thế halogen
- Trong điều kiện nhiệt độ và với sự có mặt của chất xúc tác sắt và cumen, chúng phản ứng với Br2 khan. Kết quả là nguyên tử brom đã được thế vào hạt nhân benzen
- Nếu phản ứng với Br2 dưới ánh sáng, nguyên tử Brom sẽ thay thế nhóm alkyl
- Dưới điều kiện nhiệt độ và xúc tác H2SO4, cumen có phản ứng thế nitro
- Phản ứng sunfua hóa
– Tham gia phản ứng cộng
Phản ứng với H2 trong điều kiện nhiệt độ và áp suất 10at với niken làm chất xúc tác
– Tham gia phản ứng oxi hóa
Đun nóng C9H12 thu được dung dịch làm mất màu thuốc tím KMnO4
- Phản ứng với oxy trong khí quyển ở nhiệt độ cao và không tiếp xúc để tạo thành cumene hydroperoxide
C6H5-CH9CH3)2 + O2 → C6H5-CH(CH3)2OO
- Nếu có H2SO4 loãng làm chất xúc tác thì peroxit sẽ phản ứng với axit tạo thành axeton và phenol:
C6H5-CH(CH3)2OOH → C6H5OH + CH3COCH3
3. Cumen được sản xuất thương mại như thế nào?
Cumen thương mại được sản xuất bằng phản ứng alkyl hóa Friedel–Crafts giữa benzen với propylene.
Gần 20% sản lượng cumol toàn cầu được sản xuất từ benzen. Trước đây, hỗn hợp axit photphoric và nhôm được sử dụng làm chất xúc tác, nhưng vào giữa những năm 1990, chất xúc tác này đã được thay thế bằng zeolit.
4. Ứng dụng nổi bật của cumene trong cuộc sống
- Dùng làm nguyên liệu trong các nhà máy sản xuất hóa chất phenol, axeton
- Ứng dụng hỗ trợ sản xuất ɑ -methylstyrene – chất trung gian hóa học dùng trong ngành nhựa, nhựa thông, chất kết dính và gạch lát sàn,…
- Dung môi cho sơn, men và chất kết dính phun
- Thành phần quan trọng của nhiên liệu động cơ có chỉ số octan cao
- Áp dụng cho các ngành sản xuất khác như cao su, thép, sắt, bột giấy hay các ngành liên quan đến quá trình oxy hóa phenol.

Cumen là gì? Cumen được dùng làm dung môi cho sơn như thế nào?
5. Thì là có nguy hiểm với con người không?
Theo Cơ quan Bảo vệ Môi trường Hoa Kỳ, cumene là hóa chất có độc tính thấp
- Một số triệu chứng có thể nhận thấy khi tiếp xúc với hóa chất bao gồm: đỏ mặt, chóng mặt, nhức đầu, v.v.
- Nếu tiếp xúc với da: gây kích ứng da, mẩn đỏ
- Có thể ảnh hưởng đến gan, phổi và thận khi tiếp xúc kéo dài
- Nếu hít phải hơi: chóng mặt, buồn ngủ và thậm chí hôn mê
- Vô tình nuốt phải: ho, đau bụng, đau họng, nôn mửa, nặng hơn có thể gây tử vong
6. Một số lưu ý cần biết để sử dụng và bảo quản cumen an toàn
6.1. Đang sử dụng
- Được trang bị đầy đủ các thiết bị bảo hộ cần thiết theo quy định an toàn như kính, găng tay,..
- Sau khi sử dụng và vận chuyển hóa chất phải rửa tay thật sạch bằng xà phòng và nước.

Những lưu ý cần biết khi sử dụng cumen
6.2. Đang lưu trữ
- Bảo quản trong hộp kín
- Luôn giữ nơi bảo quản khô ráo, thoáng mát và tránh tiếp xúc với ánh nắng mặt trời, nguồn nhiệt hoặc chất oxy hóa.
7. Một số bài tập liên quan đến cumen và dung dịch

Bài tập củng cố kiến thức về cumen
Bài tập 1: Có bao nhiêu nguyên tử cacbon trong một phân tử cumen?
Giải pháp:
Ta có công thức cấu tạo của cumen là C6H5-CH(CH3)-CH3
Như vậy ta thấy có tổng cộng 9 nguyên tử cacbon
Bài tập 2: Đốt cháy hoàn toàn 0,2 mol cumen rồi hấp toàn bộ sản phẩm vào 500ml dung dịch Ca(OH)2 2,3M để kết tủa và khối lượng dung dịch tăng lên 50,8g. Sau khi cho dung dịch Ba(OH)2 dư vào dung dịch, lượng kết tủa lại tăng lên và tổng khối lượng của hai kết tủa là 243,05g.
a) Xác định công thức phân tử (CTPT) của cumen trên. Biết cấu tạo của chất chỉ gồm hai nguyên tố C và H
b) Viết công thức cấu tạo (CTCT) của cumen trên. Được biết, nó không làm mất màu dung dịch brom nhưng khi đun nóng với hai brom dưới sự có mặt của ánh sáng sẽ tạo ra hai sản phẩm monobrom. Viết phương trình phản ứng xảy ra
Giải pháp:
a) Đưa CTPT của cumen về dạng CxHy, ta có:
- nCO2 = 0,2x = một
- nH2O = 0,1y = b
Số mol CaCO3 thu được sau lần thứ nhất = 2,3 – a
=> 44a + 18b – 100(2,3 – a) = 50,8
=> 144a + 18b = 280,8 (1)
Trong 243,05g kết tủa chứa: (a-1,15) mol BaCO3 và 1,15 mol CaCO3
=> 197(a – 1,115) + 100 x 1,15 = 243,05
=> a = 1,8, thay vào (1) ta được b = 1,2
=> x = 9 và y = 12
=> CTPT của cumen là C9H12
b) CTCT của cumen: C6H5-CH(CH3)-CH3
PTPU:
C6H5-CH(CH3)-CH3 + Br2 → C6H5-CBr(CH3)-CH3 + HBr
Bài tập 3: Để sản xuất 1 tấn cumene cần sử dụng bao nhiêu m3 (ở điều kiện tiêu chuẩn) hỗn hợp khí tách ra khỏi khí crackinh gồm 60% propylene và 40% propane (theo thể tích)? Được biết, hiệu suất phản ứng đạt 80%.
Giải pháp:
Ta có nC3H5 = ncumen = 106/120 mol
=> VC3H6 = (106/120)22,4 ≈ 186666,7L ≈ 187,7 m3
=> Vhh = (186,7 x 100%)/ 60% ≈ 311 m3
H = 80% => Vhh = (311 x 100%)/ 80% = 388,75 m3
Hy vọng với bài viết trên Labvietchem đã giúp bạn đọc hiểu rõ hơn về cumen là gì cũng như những đặc tính, ứng dụng nổi bật của nó. Hãy liên hệ ngay với chúng tôi bằng cách gọi tới số nóng 0826 020 020 hoặc để lại bình luận ngay bên dưới bài viết nếu bạn còn thắc mắc nào liên quan.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn