Nội dung bài viết
Chất khử hay còn gọi là chất khử, đóng vai trò là chất cho điện từ trong các phản ứng oxi hóa khử. Nó đóng một vai trò quan trọng trong nhiều quá trình oxy hóa khử và điện phân của các chất. Hãy cùng LabTrường Chu Văn An tìm hiểu chất khử là gì? Vai trò của nó trong các phản ứng oxi hóa khử.
1. Chất khử là gì?
Chất khử hay còn gọi là chất khử hoặc chất oxy hóa là một nguyên tố hóa học có trong các phản ứng oxi hóa khử làm khử một chất khác.
Trong các phản ứng oxi hóa khử, nó là chất cho điện tử (chất cho điện tử), chẳng hạn như phản ứng hóa học sau:
2Zn(rắn) + O2 → 2Zn2+ (rắn) + 2O2-

Chất khử là gì?
Chất khử trong phản ứng trên là kẽm. Kẽm nhường 2 electron hóa trị và trở thành 1 ion, tạo thành hợp chất ổn định với oxy.
Phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự trao đổi electron giữa các chất tham gia dẫn đến sự thay đổi số oxi hóa của một số nguyên tố. Trong phản ứng này, chất bị oxy hóa mất electron, còn chất khử thu được electron. Phản ứng hóa học này đóng một vai trò quan trọng trong tự nhiên và trong các ứng dụng công nghiệp.
2. Điểm mạnh và điểm yếu của chất khử
Chất khử mạnh là chất dễ mất hoặc nhường electron. Hạt nhân nguyên tử có xu hướng hút các electron xung quanh. Đối với các nguyên tố có bán kính nguyên tử lớn thì khoảng cách từ hạt nhân đến electron càng xa và lực hấp dẫn của hạt nhân càng yếu. Vì vậy, các nguyên tố này thường có tính khử cao hơn. Ngoài ra, các nguyên tố có độ âm điện thấp có khả năng thu hút các electron liên kết của các nguyên tử hoặc phân tử yếu hơn. Năng lượng ion hóa tương đối thấp của chúng cũng góp phần làm cho chúng trở thành chất khử mạnh. Khả năng khử của một số chất khử thông dụng được thể hiện trong bảng dưới đây:
|
Chất khử |
Khả năng khử (V) |
|
Lý |
-3.04 |
|
Na |
-2,71 |
|
Mg |
-2,38 |
|
Al |
-1,66 |
|
H2(khí) + 2OH – |
-0,83 |
|
Cr |
-0,74 |
|
Fe |
-0,41 |
|
H2 |
0,00 |
|
Sn2+ |
+0,15 |
|
Củ |
+0,16 |
|
Ag |
+0,80 |
|
2Br- |
+1,07 |
|
2Cl- |
+1,36 |
|
Mn2+ + 4H2O |
+1,49 |
Một số chất khử mạnh điển hình như kim loại kiềm, kiềm thổ bao gồm: Kali, canxi, bari, natri, magie và các hợp chất chứa ion H-,…
Mỗi nguyên tố có thể đóng vai trò là chất khử hoặc chất oxy hóa, tùy thuộc vào điều kiện phản ứng.
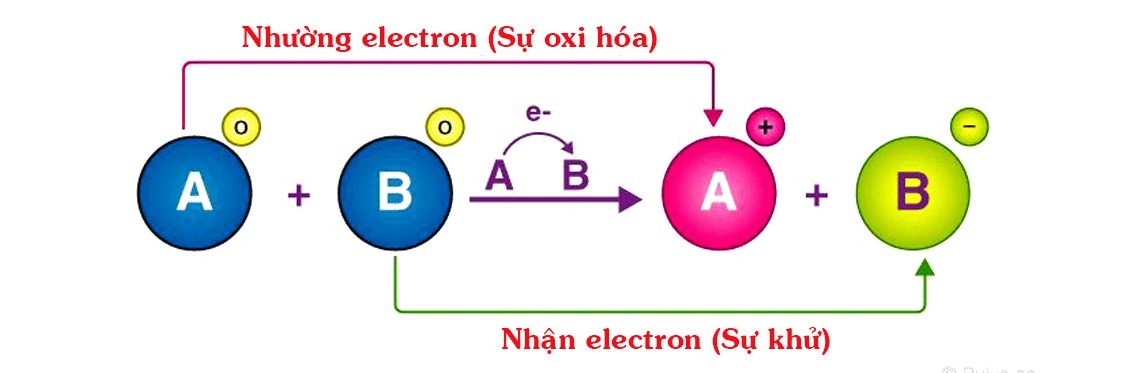
Chất khử và chất oxi hóa
3. Phân loại chất khử
3.1. Chất khử hữu cơ
Chất khử hữu cơ là những hợp chất hữu cơ có khả năng nhường electron, giúp oxy hóa các chất khác trong các phản ứng hóa học. Chúng thường chứa các nguyên tử carbon và hydro, kết hợp với các nguyên tử khác như oxy, nitơ, lưu huỳnh và halogen.
Cấu trúc của chất khử hữu cơ có thể là các hợp chất đơn giản như hydrocacbon (chỉ chứa cacbon và hydro) hoặc các hợp chất phức tạp hơn như rượu, aldehyd, xeton và axit cacboxylic.
Tính chất của chất khử hữu cơ bao gồm khả năng mất electron, khả năng hình thành liên kết hóa học, tính chất axit-bazơ và khả năng phản ứng. Chúng có thể tham gia vào các phản ứng oxi hóa khử, phản ứng thay thế và phản ứng cộng.
Chất khử hữu cơ có nhiều vai trò trong đời sống như sản xuất dược phẩm, chất tẩy rửa, chất bảo quản thực phẩm và trong quá trình tổng hợp các hợp chất quan trọng khác.
3.2. Chất khử vô cơ
Chất khử vô cơ là chất cho điện tử, làm giảm số oxi hóa của chất đó, bao gồm kim loại, ion hydrit (H-) và muối khử.
Chất khử vô cơ có ứng dụng quan trọng trong các phản ứng hóa học và quá trình khử.
4. Tầm quan trọng của chất khử trong phản ứng hóa học
Các chất khử và chất oxy hóa có thể gây ra sự ăn mòn điện, đó là “sự hư hỏng của kim loại do phản ứng điện hóa”. Quá trình này đòi hỏi sự tham gia của các ion đóng vai trò là chất nhận điện tích (ion dương) và các ion đóng vai trò là chất cho điện tích (ion âm). Cực dương là điện cực nơi xảy ra quá trình oxy hóa, do chất khử mất electron ở đây, trong khi cực âm là điện cực diễn ra quá trình khử, do chất oxy hóa nhận electron. Ăn mòn điện hóa xảy ra khi có sự khác biệt về thế oxy hóa giữa hai khu vực. Khi điều này xảy ra, kim loại ở cực dương sẽ bắt đầu bị ăn mòn dần do hình thành mạch kín xuyên qua chất điện phân.
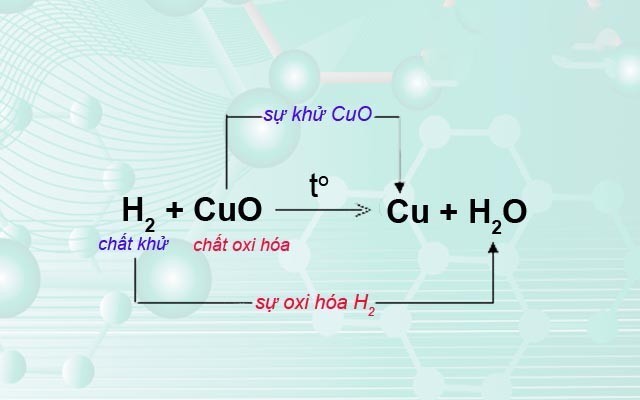
Phản ứng oxi hóa khử
Trên đây là những chia sẻ của LabvietCHEM về chất khử và tầm quan trọng của chúng trong các phản ứng hóa học. Nếu có bất kỳ thắc mắc hay thắc mắc nào, vui lòng để lại bên dưới phần bình luận để chúng tôi giải đáp.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn