Nội dung bài viết
Bạc Nitrat là một hợp chất hóa học được sử dụng trong nhiều lĩnh vực của đời sống. Vậy bạc Nitrat là gì? Nó có thuộc tính không và tại sao? Và có những ứng dụng đặc biệt nào? Hãy cùng LabTrường Lê Hồng Phong tìm hiểu qua bài viết sau đây nhé!
1. Bạc Nitrat là gì?
Bạc Nitrat hay còn gọi là bạc đơn sắc, muối axit nitric,… là hợp chất phổ biến của axit nitric. Công thức hóa học của nó là AgNO3, có tính oxy hóa và ăn mòn.
Hợp chất hóa học này thường được sử dụng để mạ bạc, nhuộm tóc, phản xạ, kiểm tra ion bromide, ion iodide và ion clorua…, hoặc thậm chí trong in ấn và hóa học.
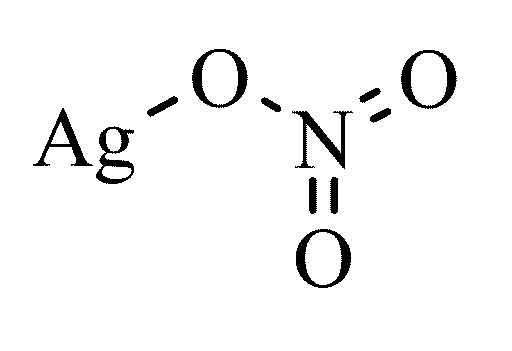
Cấu trúc phân tử của Bạc nitrat – AgNO3
2. Tìm hiểu tính chất lý hóa của Bạc Nitrat
3.1 Tính chất vật lý của bạc nitrat – AgNO3
- Bạc Nitrat là một tinh thể dễ vỡ, trong suốt, không màu.
- Tan nhanh trong nước và amoniac, ít tan trong etanol khan và hầu như không tan trong HNO3 đậm đặc.
- AgNO3 có tính axit yếu nhưng có tính oxy hóa mạnh và có tính ăn mòn nhất định.
- Mật độ: 5,35 g/cm3
- Điểm sôi: 444 °C (717 K; 831 °F)
- Nhiệt độ nóng chảy: 212 °C (485 K; 414 °F)

Bạc Nitrat là tinh thể dễ vỡ, trong suốt, không màu
3.2 Tính chất hóa học của bạc nitrat – AgNO3
* Phản ứng oxi hóa khử:
AgNO3 có thể bị khử thành bạc nguyên tố bằng các chất khử trung bình hoặc mạnh:
N2H4 + 4AgNO3 → 4Ag + N2 + 4HNO3
H3PO3 + 2AgNO3 + H2O → 2Ag + H3PO4 + 2HNO3
* Phản ứng phân hủy AgNO3:
AgNO3 → 2Ag + 2NO2 + O2
* AgNO3 phản ứng với NH3:
2AgNO3 + 2NH3 · H2O → Ag2O + H2O + 2NH4NO3 (một lượng nhỏ amoniac)
AgNO3 + 3NH3 · H2O → Ag(NH3)2OH + NH4NO3 + 2H2O (dư lượng amoniac)
* Bạc nitrat phản ứng với axit:
AgNO3 + HCl → AgCl + HNO3
HBr + AgNO3 → AgBr + HNO3
* Bạc nitrat phản ứng với NaOH:
2NaOH + 2AgNO3 → 2NaNO3 + Ag2O + H2O
* Bạc nitrat phản ứng với khí clo:
Cl2 + H2O → HCl + HClO HCl + AgNO3 → AgCl + HNO3
4. Cách điều chế Bạc Nitrat – AgNO3
Người ta có thể điều chế AgNO3 theo phương trình phản ứng sau:
3 Ag + 4 HNO3(lạnh và loãng) → 3 AgNO3 + 2 H2O + NO
3 Ag + 6 HNO3 (đậm đặc, nóng) → 3 AgNO3 + 3 H2O + 3 NO2
Tùy theo nồng độ HNO3 mà sản phẩm phụ sinh ra sẽ khác nhau. Do nitơ oxit sinh ra trong phản ứng khá nguy hiểm nên quá trình điều chế AgNO3 cần phải thực hiện trong tủ hút.
5. Ứng dụng Bạc Nitrat- AgNO3 trong nhiều lĩnh vực
– Đối với hóa phân tích: AgNO3 được dùng để kết tủa ion clorua và hiệu chuẩn dung dịch NaCl.
– Đối với các ngành công nghiệp:
- Bạc Nitrat được dùng để sản xuất các loại muối bạc khác.
- Bạc nitrat được sử dụng để sản xuất chất kết dính dẫn điện, sàng phân tử A8x, máy lọc không khí mới, quần áo và găng tay cân bằng áp suất mạ bạc.
- Bạc Nitrat được sử dụng làm vật liệu nhạy sáng cho phim, phim chụp ảnh và phim X-quang.
- AgNO3 được dùng để mạ bạc các linh kiện điện tử, sản phẩm thủ công mỹ nghệ, gương, bình giữ nhiệt.
- AgNO3 còn được sử dụng trong sản xuất pin kẽm-bạc.
– Đối với y học: Bạc Nitrat dùng để ăn mòn mô hạt tăng sinh. Dung dịch AGNO3 pha loãng được dùng làm thuốc diệt nấm trị nhiễm trùng mắt.
– Một số ứng dụng khác:
- Bạc Nitrat được sử dụng để phát hiện aldehyd và đường.
- Dùng để đo ion clorua, mạ điện, tạo màu gốm, chụp ảnh, xúc tác xác định mangan.

AgNO3 được dùng để mạ bạc nhiều sản phẩm
6. Bạc nitrat – AgNO3 có phải là chất độc không?
Vai trò của Bạc Nitrate trong cuộc sống là điều chúng ta không thể phủ nhận. Tuy nhiên, nó có nhiều đặc điểm của chất độc:
- Chất oxy hóa mạnh, nhóm 2, H272
- Có khả năng ăn mòn kim loại, nhóm 1, H290
- Có khả năng ăn mòn da, nhóm 1B, H314
- Đối với môi trường nước, AgNO3 gây tác hại cấp tính và mãn tính
Vì vậy, khi sử dụng bạc nitrat nếu tiếp xúc trực tiếp với cơ thể có thể gây ra những tổn thương như:
- Tiếp xúc với da sẽ gây kích ứng, có thể gây viêm da và bỏng.
- Nước bắn vào mắt có thể gây kích ứng, đục giác mạc, bỏng kết mạc và mù lòa.
- Hít phải AgNO3 có thể gây kích ứng đường hô hấp, thở khò khè, khó thở, viêm thanh quản, nhức đầu, nôn mửa…
- Nuốt phải bạc nitrat sẽ gây bỏng hệ hô hấp trên và vòm miệng, đau bụng dữ dội, nôn ra chất đen, tiêu chảy, viêm nướu, kích động, nặng hơn sẽ ảnh hưởng đến thận và phổi.

Nuốt phải AgNO3 sẽ gây đau bụng dữ dội và nôn ra chất đen
7. Một số lưu ý khi sử dụng Silver Nitrate an toàn
- Cần trang bị đầy đủ các thiết bị chống độc khi làm việc với AgNO3 như quần áo bảo hộ, găng tay, khẩu trang, kính,…
- Trường hợp AgNO3 tiếp xúc với da phải cởi bỏ ngay quần áo bị nhiễm bẩn và rửa lại da nhiều lần bằng nước sạch.
- Nếu mắt tiếp xúc với bạc Nitrate, bạn cần tháo kính áp tròng (nếu có) và rửa sạch nhiều lần với nước.
- Nếu nuốt phải AgNO3, nạn nhân cần được cho uống nước và đưa đến cơ sở y tế cấp cứu.
Nếu AgNO3 tiếp xúc với da phải rửa sạch da nhiều lần bằng nước sạch
Trên đây là những kiến thức hữu ích về Bạc Nitrat. Hy vọng bài viết này sẽ giúp bạn hiểu rõ hơn về hợp chất hóa học này. Nếu bạn có thắc mắc gì về Bạc Nitrat, vui lòng liên hệ LabiệtChem để được giải đáp!
Ngoài ra, nếu bạn đang có nhu cầu về hóa chất, thiết bị phòng thí nghiệm vui lòng tham khảo sản phẩm tại website của LabTrường Chu Văn An hoặc liên hệ số HOTLINE: 0826.020.020 để nhận được tư vấn. LabTrường Chu Văn An – nhà cung cấp thiết bị phòng thí nghiệm uy tín hàng đầu hiện nay – luôn mong muốn mang đến cho khách hàng những sản phẩm tốt nhất!


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn