Nội dung bài viết
Axit formic là sản phẩm của quá trình tổng hợp hóa học và cũng có sẵn trong tự nhiên, chủ yếu có trong nọc ong và vết đốt của kiến. Để hiểu rõ hơn axit formic là gì? Các tính chất vật lý và hóa học là gì? Các ứng dụng thực tế của axit formic là gì? Hãy theo dõi bài viết dưới đây để có được những thông tin hữu ích nhé.

Axit formic là gì?
Axit formic là gì?
– Axit formic là dạng đơn giản nhất của hợp chất hữu cơ axit cacboxylic có công thức HCOOH hoặc CH2O2. Trong tự nhiên, chúng ta có thể tìm thấy axit formic trong nọc ong và vết đốt của côn trùng có cánh, chủ yếu là kiến.
– Một số tên gọi khác: axit methanoic, axit aminonic, aldehyt formic, axit formic, axit cacboxylic hydro, axit formylic,…
– Tên axit formic xuất phát từ tiếng Latin: ant – formica. Nó có thể dễ dàng tách ra khỏi quá trình chưng cất xác kiến.

Axit formic có trong nọc ong
Tính chất vật lý và hóa học của axit formic
1. Tính chất vật lý
– Là chất lỏng không màu, có mùi đặc trưng, dễ bốc khói.
– Axit formic tan trong nước và các dung môi hữu cơ khác và ít tan trong hydrocacbon.
– Trong hydrocacbon và ở pha hơi, axit formic bao gồm các dime liên kết hydro chứ không phải là các phân tử riêng lẻ, và trong pha khí, liên kết hydro này tạo ra sự sai lệch lớn so với định luật khí lý tưởng.
– Phân tử: 46,0254g/mol.
– Nhiệt độ nóng chảy: 8,4 độ C.
– Nhiệt độ sôi: 100,8 độ C.
2. Tính chất hóa học
+> Tính chất của axit
Mặc dù axit formic là một axit yếu nhưng nó mạnh nhất trong dãy tương đồng của axit cacboxylic bão hòa, đơn chức, mạch hở và do hiệu ứng tích lũy mật độ electron trong nhóm –COOH nên nó mạnh hơn axit cacbonic H2CO3. Nó có tất cả các tính chất của một axit, bao gồm:
– Dung dịch axit formic làm quỳ tím chuyển sang màu đỏ nhạt.
– Phản ứng với kim loại mạnh tạo thành khí hiđro theo phương trình phản ứng:
2NA + 2HCOOH → 2HCOONA + H2
– Phản ứng với oxit bazơ theo phương trình phản ứng
CUO + 2HCOOH → (HCOO)2CU + H2O
– Phản ứng với bazơ theo phương trình phản ứng
NAOH + HCOOH → HCOONA + H2O
– Phản ứng với muối của axit yếu theo phương trình phản ứng
NAHCO3 + HCOOH → HCOONA + CO2 + H2O
+> Tính chất của nhóm – COOH
– Phản ứng este hóa (xúc tác bằng axit sunfuric đậm đặc và nhiệt độ)
HCOOH + CH3OH → HCOOCH3 + H2O
Phản ứng này có thể đảo ngược.
– Tính aldehyd
Phản ứng gương: Khi nhóm chức aldehyd phản ứng với AgNO3 hoặc Ag2O trong môi trường amoniac sẽ tạo ra bạc.
HCOOH + 2[Ag(NH3)2]OH → (NH4)2CO3 + 2Ag↓ + 2NH3↑ + H2O
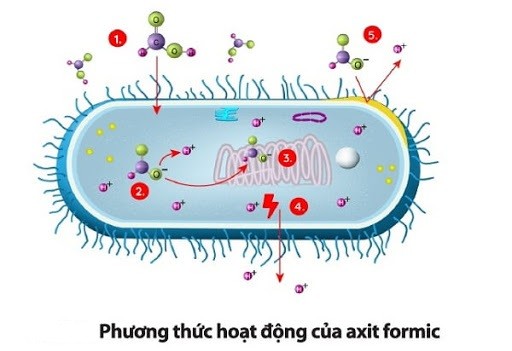
Dựa vào tính chất trên, chúng ta có thể phân biệt axit formic và axit axetic bằng phản ứng gương với thuốc thử AgNO3/NH3:
+ Axit formic sẽ xuất hiện kết tủa bạc do có nhóm aldehyt (-CHO).
+ Nếu không có hiện tượng xảy ra thì đó là axit axetic (CH3COOH).
Phương pháp điều chế axit formic
Axit formic là sản phẩm phụ của quá trình sản xuất các hóa chất khác, điển hình là axit axetic. Tuy nhiên, lượng axit formic thu được không đủ đáp ứng nhu cầu hiện nay. Do đó, nó được chuẩn bị theo nhiều cách:
1. Trong phòng thí nghiệm
– Cách 1: Đun nóng axit oxalic trong glycerol khan rồi hấp để chiết axit formic.
– Cách 2: Thủy phân axit etyl isonitrile bằng xúc tác HCl
C2H5NC + 2H2O→ C2H5NH2 + HCOOH
2. Trong công nghiệp
Phản ứng metanol với cacbon monoxit (được xúc tác bởi bazơ mạnh) để tạo ra metyl formate, một dẫn xuất của axit formic. Phản ứng này được thực hiện ở pha lỏng trong điều kiện áp suất cao, nhiệt độ 80 độ C, áp suất 40 atm.
CH3OH + CO → HCOOCH3
Phản ứng metyl formate với amoniac để tạo ra formamit và sau đó thủy phân formamit bằng axit sulfuric để tạo ra axit formic
HCOOCH3 + NH3 → HCONH2 + CH3OH
HCONH2 + H2O + ½H2SO4 → HCOOH + ½(NH4)2SO4
HCOOCH3 + H2O → HCOOH + CH3OH
Nhược điểm của phương pháp này là nó tạo ra sản phẩm phụ là amoni sunfat. Hiện nay, nhiều nhà sản xuất đã sử dụng công nghệ BASF để tách nước khỏi axit formic bằng cách chiết chất lỏng bằng bazơ hữu cơ.
Axit formic có những ứng dụng gì?
– Dùng trong công nghiệp dệt nhuộm, cao su, thuốc trừ sâu, tổng hợp hóa học… Đây là loại axit hữu cơ hiệu quả và an toàn với môi trường.
– Là chất trung hòa và điều chỉnh độ pH trong sản xuất dệt may.
– Là axit dùng để thuộc da.

Là một axit cho da thuộc da
– Kết hợp với hydrogen peroxide để tạo thành chất epoxid hóa dầu đậu.
– Là dung dịch tẩy cặn, diệt khuẩn trong vệ sinh, lau chùi nhà cửa và sản xuất công nghiệp.
– Được sử dụng làm chất điều chỉnh giá trị pH trong khử lưu huỳnh khí thải, đông tụ mủ và nhiều ứng dụng khác.
– Giúp ủ thức ăn cho vật nuôi và được chọn làm giải pháp thay thế hiệu quả kháng sinh trong chăn nuôi.

Là giải pháp thay thế kháng sinh trong chăn nuôi
– Cung cấp hydrua trong nhiều quá trình hóa học khác nhau.
– Trong lĩnh vực dầu khí:
+ Axit formic giúp hòa tan canxi cacbonat.
+ Muối của axit formic là kali fomat dùng trong giếng dầu, có tác dụng làm tan băng.
– Axit Formic được sử dụng làm dược chất hoạt tính trong sản xuất thuốc.
Là dược chất có hoạt tính trong sản xuất thuốc
Lưu ý, bảo quản khi sử dụng axit formic
1. Lưu ý khi sử dụng
– Khi làm việc với axit formic cần trang bị đầy đủ quần áo bảo hộ, găng tay, kính mắt,… để tránh axit bắn vào người.
– Hóa chất này có thể nguy hiểm khi sử dụng ở nồng độ cao do tính chất ăn mòn của axit.
– Nếu vô tình chạm vào hoặc hít phải có thể gây ra các triệu chứng loét, buồn nôn, bỏng, mụn rộp tại chỗ bám dính. Trong trường hợp đường hô hấp bị ảnh hưởng, người bệnh cần được đưa ra nơi thoáng đãng và liên hệ ngay với nhân viên y tế để được điều trị thích hợp.
2. Bảo quản
– Bảo quản nơi khô ráo, thoáng mát, nhiệt độ phòng dưới 30 độ C.
– Tránh đặt gần nguồn nhiệt, lửa để tránh cháy nổ.
Qua bài viết trên chúng tôi đã giúp các bạn giải đáp được câu hỏi Axit formic là gì cũng như giải đáp thắc mắc về tính chất lý hóa và ứng dụng của axit formic trong thực tế. Nếu bạn có thắc mắc về axit formic hoặc muốn mua hóa chất vui lòng liên hệ Labvietchem theo số hotline 0826 020 020 để được hỗ trợ tốt nhất.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn