Nội dung bài viết
Axit Fluoroantimonic là một axit cực mạnh, thường tồn tại ở dạng H2SbF7. Nó được sử dụng trong sản xuất các hợp chất vàng tetraxenon. Hãy cùng LabTrường Chu Văn An tìm hiểu thêm về axit fluoroantimonic là gì? Tính chất vật lý, hóa học và ứng dụng của chúng trong đời sống.
1. Axit fluoroantimonic là gì?
Axit Fluoroantimonic là một axit vô cơ, có công thức hóa học chung là xHF·ySbF5. Nó thường tồn tại dưới dạng H2SbF7 (hoặc 2HF·SbF5, HSbF6 hoặc đơn giản là HF-SbF5.
Tên danh pháp IUPAC: Axit Fluoroantimonic.
Tên hệ thống: Fluoranium hexafluorostibanuide, Fluoranium hexafluoridoantimonate(1−)
Axit Fluoroantimonic là một siêu axit, được điều chế từ phản ứng giữa hydro florua (HF) với antimon pentaflorua (SbF5) theo tỷ lệ 2:1.
Hóa chất này được sử dụng trong quá trình tổng hợp các hợp chất hữu cơ và sản xuất các hợp chất vàng tetraxenon.
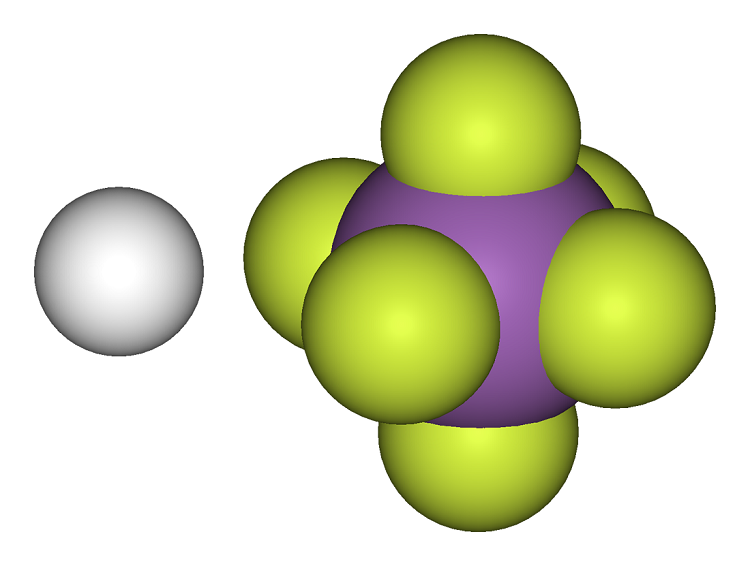
Hình 1: Cấu trúc của axit fluoroantimonic
2. Tính chất đặc trưng của axit fluoroantimonic
2.1. Tính chất vật lý
– Cảm giác: Tồn tại ở dạng lỏng, không màu.
– Khối lượng phân tử: 256,76168 g/mol.
– Tỷ trọng: 2,885 g/cm³.
– Độ hòa tan:
+ Hòa tan trong nước.
+ Tan trong SO2ClF, SO2.
– Độ axit: pKa=-25.
– Tính cơ bản: pKb=39.

Hình 2: Axit Fluoroantimonic
2.2. Tính chất hóa học
Khi đun nóng axit fluoroantimonic, nó sẽ phân hủy thành khí hydro florua tự do và pentaflorua antimon lỏng. Ở nhiệt độ thấp khoảng 40oC, axit fluoroantimonic sẽ giải phóng HF dưới dạng khí. Để thu hồi pentaflorua antimon lỏng từ axit fluoroantimonic, có thể thực hiện đun nóng để giải phóng khí HF.
3. Điều chế axit fluoroantimonic bằng phương pháp nào?
Để điều chế axit fluoroantimonium, hydro florua (HF) được xử lý bằng pentaflorua antimon (SbF5). Phương trình diễn ra như sau:
SbF5 + 2HF → SbF6- + H2F+
4. Ứng dụng của axit fluoroantimonic trong đời sống
Trong thực tế hiện nay, siêu axit cực mạnh này được sử dụng rộng rãi, đặc biệt là trong lĩnh vực kỹ thuật hóa học và hóa học hữu cơ. Năm 1967, Hogeveen và Bickel công bố rằng axit fluoroantimonic có khả năng loại bỏ H2 khỏi isobutane và loại bỏ metan khỏi neopentane. Siêu axit này có khả năng proton hóa các hợp chất hữu cơ bất kể dung môi của chúng.
Phản ứng hóa học:
(CH3)3CH + H+ → (CH3)3C+ + H2↑
(CH3)4C + H+ → (CH3)3C+ + CH4↑
Ngoài ra, axit fluoroantimonic còn gây mất nước, khử hydro và tạo ra hầu hết các hợp chất hữu cơ. Vì vậy, axit này được sử dụng trong quá trình sản xuất hợp chất vàng tetraxenon. Các vật liệu tương thích với axit fluoroantimonic làm dung môi bao gồm: SO2ClF, sulfur dioxide và một số chlorofluorocarbon. Axit Fluoroantimonic cũng được sử dụng trong quá trình tổng hợp và xác định đặc tính của cacbocation, đồng thời làm chất xúc tác trong quá trình kiềm hóa và acyl hóa trong hóa dầu.
>> Xem thêm: TOP 06 axit mạnh nhất bạn cần biết.
5. Những lưu ý khi sử dụng và bảo quản axit fluoroantimonic
HF-SbF5 là chất cực kỳ ăn mòn và độc hại, nhạy cảm với độ ẩm. Giống như hầu hết các axit mạnh, axit hydrofluoric phản ứng mạnh với nước do quá trình hydrat hóa tỏa nhiệt. Chỉ có thể sử dụng hydro florua làm dung môi cho axit này vì không thể sử dụng nước. Đun nóng axit fluoroantimonic cũng nguy hiểm vì nó phân hủy thành khí florua độc hại. Phương pháp bảo quản duy nhất là bảo quản trong hộp chứa PTFE-Teflon, vì thủy tinh sẽ tan chảy khi tiếp xúc. Khi xử lý hoặc ở gần chất ăn mòn này, phải luôn đeo thiết bị bảo hộ vì axit fluoroantimonic có thể ăn mòn xương và phản ứng dữ dội với nước trong cơ thể con người.

Hình 3: Axit Fluoroantimonic có tính ăn mòn cực cao
Trên đây là những chia sẻ của LabTrường Chu Văn An về tính chất, phương pháp điều chế và ứng dụng của axit fluoroantimonic. Nếu có thắc mắc gì hãy để lại thông tin của bạn bên dưới phần bình luận để chúng tôi giải đáp nhé.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn