Nội dung bài viết
Bạn đã bao giờ nghe đến cái tên amin chưa? Bạn đã từng tìm hiểu về đặc tính và ứng dụng của chất này chưa? Không cần phải tìm đâu xa, hôm nay chúng ta hãy cùng LabENGCHEM tìm hiểu về amin nhé? Nó ở đâu và nó hoạt động với chất gì?
1. Tìm hiểu Amin là gì?
Đây là hợp chất hữu cơ, khi một hoặc nhiều nguyên tử hydro trong phân tử NH3 được thay thế bằng gốc hydrocarbon.
Ví dụ, amin là một hợp chất hữu cơ thay thế một hoặc nhiều nguyên tử hydro trong phân tử NH3 bằng gốc hydrocarbon.
Ví dụ: CH3-NH2; CH3-NH-CH3, CH3-N-CH3, CH2=CH-CH2-NH2, C6H5NH2.

Amin là gì?
2. Phân loại amin
2.1. gốc hydrocacbon
– Amin béo: CH3NH2, C2H5NH2
– Amin thơm: CH3C6H4NH2, C6H5NH2, …
– Amin dị vòng
2.2. Theo hàm lượng amin
Vậy hàm lượng amin là bao nhiêu? Mức amin là số nguyên tử H trong phân tử NH3 được thay thế bằng gốc hydrocarbon. Theo đó, amin sẽ được phân loại thành:
+ Amin bậc 1: R-NH2 (Aliphatic bậc 1 phản ứng với axit nitơ tạo thành rượu tương ứng và giải phóng khí N2)
Ví dụ: CH3-CH2-CH2-NH2
C2H5-NH2 + HONO -> C2H5OH + N2 + H2O (xúc tác HCl)
+ Amin bậc hai: R-NH-R’ (Amin bậc cấp béo và thơm phản ứng với axit nitơ tạo ra nitrosamine là chất có màu vàng, nhờ đó phân biệt được amin bậc hai với amin bậc một)
Ví dụ:
CH3-CH2-NH-CH3
(CH3)2N-H + HONO -> CH3)2N-N=O + H2O
+ Amin bậc ba: Amin bậc ba béo không phản ứng với axit nitơ hoặc chỉ tạo thành muối không ổn định, dễ bị thủy phân. Các amin bậc ba thơm phản ứng với axit nitro để tạo ra các sản phẩm thay thế thơm. (CH3)3N amin bậc ba
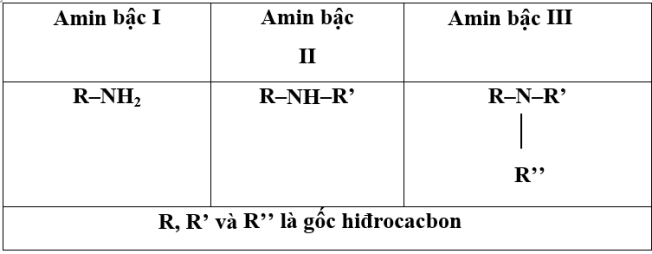
Amin được chia thành amin bậc 1, bậc 2 và bậc 3
2.3. Công thức của amin
– Amin đơn chức: CxHyN
– Amin đơn chức bão hòa: CnH2n+1NH2 hoặc CnH2n+3N
– Polyamin bão hòa: CnH2n+2-z(NH2)z hoặc CnH2n+2+zNz
3. Cách gọi tên và danh pháp các amin
3.1. Cách gọi tên amin theo danh pháp hàm gốc
– Tên bazơ hiđrocacbon + amin
Ví dụ: C2H5-NH2 (Ethylamine), CH3NH2 (metylamine), CH3CH(NH2)CH3 (isopropylamine),…
3.2. Cách đặt tên bằng danh pháp thay thế
– Tên hydrocarbon + vị trí + amin
Ví dụ: CH3NH2 đọc là methanamine, C2H5-NH2 (Etanamin), CH3CH(NH2)CH3 (propan-2-amine)
– Tên gọi thường chỉ áp dụng cho một số amin:
Hợp chất: CH3NH2 (tên gốc là methylamine, tên thay thế là methanamine)
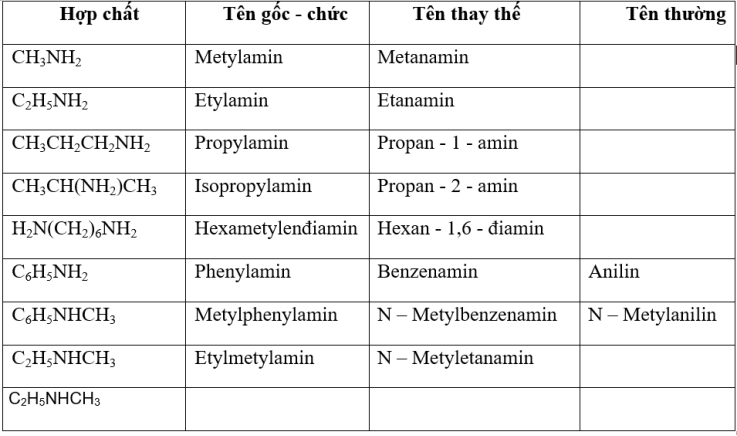
Cách đọc tên ghép
Lưu ý: Tên các nhóm alkyl thường sẽ được đọc theo thứ tự a, b, c,… + amin.
Đối với amin bậc hai và bậc ba chọn chuỗi dài nhất chứa N làm chuỗi chính
– Nếu có 2 nhóm alkyl thì thêm chữ N vào đầu
Ví dụ: CH3-NH-C2H5: N sẽ đọc là N etyl dimethyl amin
– Nếu có 3 nhóm alkyl khác nhau sẽ có 2 chữ cái N cách nhau 1 tên alkyl
Ví dụ: CH3-N(C2H5) -C3H7: N – etyl-N-metyl propyl propyl amin
– Khi nhóm -NH2 đóng vai trò tích cực thì gọi là nhóm amino.
Ví dụ: CH3CH(NH2)COOH (axit 2-amino propanoic)
3.3. Đồng phân của amin
– Đồng phân chuỗi cacbon
– Đồng phân vị trí nhóm chức
– Đồng phân bậc của amin
4. Tính chất vật lý của amin
Amin có khả năng hòa tan tốt trong nước, do giữa nước và amin có liên kết hydro liên phân tử nên độ hòa tan trong nước giảm khi số nguyên tử C tăng.
Methyl-, dimethyl-, trimethyl-, ethylamine là các chất khí có mùi khó chịu, độc hại và dễ tan trong nước. Các amin tương đồng cao hơn là chất lỏng hoặc chất rắn.
Anilin là chất lỏng, nhiệt độ sôi 184 độ C, không màu, rất độc, ít tan trong nước, tan trong rượu và benzen.
5. Tính chất của chức amin
– Tính bazơ tác dụng lên giấy quỳ đỏ ẩm hoặc phenolphtalein và phản ứng với axit.
– Dung dịch methylamine và nhiều chất tương tự có khả năng làm quỳ tím chuyển màu xanh hoặc chuyển phenolphtalein thành màu hồng do lực liên kết proton mạnh hơn amoniac.
– Anilin và amin thơm thường rất khó tan trong nước. Dung dịch này không làm đổi màu quỳ tím và phenolphtalein.
– Phản ứng với axit nitro
+ Amin bão hòa bậc 1 + HNO2 -> ROH + N2 + H2O
Ví dụ:
C2H5NH2 + NONO -> C2H5OH + N2 + H2O
+ Amin thơm bậc một phản ứng với HNO2 ở nhiệt độ thấp tạo thành muối diazoni.
Ví dụ:
C6H5NH2 + HONO + HCl -> C6H5N2 + Cl- + 2H2O
+ Phản ứng alkyl hóa: amin bậc một hoặc bậc hai phản ứng với alkyl halogenua (CH3l,…)
+ Phản ứng này dùng để điều chế các amin bậc cao từ các amin bậc thấp hơn.
C2H5NH2 + CH3I -> C2H5NHCH3 + HI
+ Phản ứng của amin tan trong nước với dung dịch muối của kim loại có kết tủa hydroxit
3CH3NH2 + FeCl3 + 3H2O -> Fe(OH)3 + 3CH3NH3Cl
+ Amin có phản ứng thế ở vòng thơm của anilin
6. Ứng dụng của amin

Amin là chất trung gian trong quá trình điều chế các chất
– Bởi vì hầu hết các amin hiện nay được sử dụng rộng rãi làm chất trung gian để điều chế các chất khác có ứng dụng quan trọng hơn, đặc biệt là axit amin, thuốc nhuộm, chất lưu hóa cao su… chỉ một số ít có hoạt tính sinh học.
Ví dụ: Một số là vitamin: ví dụ thiamine clorua (1 dạng B1, pyridoxine vit B6)
– Amphetamine kích thích hệ thần kinh trung ương, làm tăng huyết áp và mạch nhưng gây nghiện.
– Chloropheniramine là một trong những thành phần có trong thuốc cảm
– Chlorodiazeppoxide có tác dụng an thần
– Novocain và demerol – khá nổi tiếng vì liên quan tới cái chết của Michael Jackson, được dùng làm thuốc gây mê, giảm đau.
Trên đây là thông tin về Amin là gì?đặc điểm và ứng dụng của nó. Hãy theo dõi các bài viết tiếp theo của LabTrường Lê Hồng Phong để theo dõi các bài viết thú vị tiếp theo nhé.
Tham khảo hóa chất phòng thí nghiệm


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn