Nội dung bài viết
Bạn có biết thành phần chính của gas (LPG) dùng để nấu ăn trong nhà bếp hay xăng cung cấp năng lượng cho xe máy là gì không? Đó là Ankan. Ankan là một trong những hợp chất hữu cơ đơn giản nhất nhưng có vai trò cơ bản và ứng dụng vô cùng rộng rãi trong đời sống và công nghiệp.
Hãy cùng ENGCHEM tìm hiểu về hợp chất quan trọng này nhé!
1. Ankan là gì và công thức chung của nó là gì?
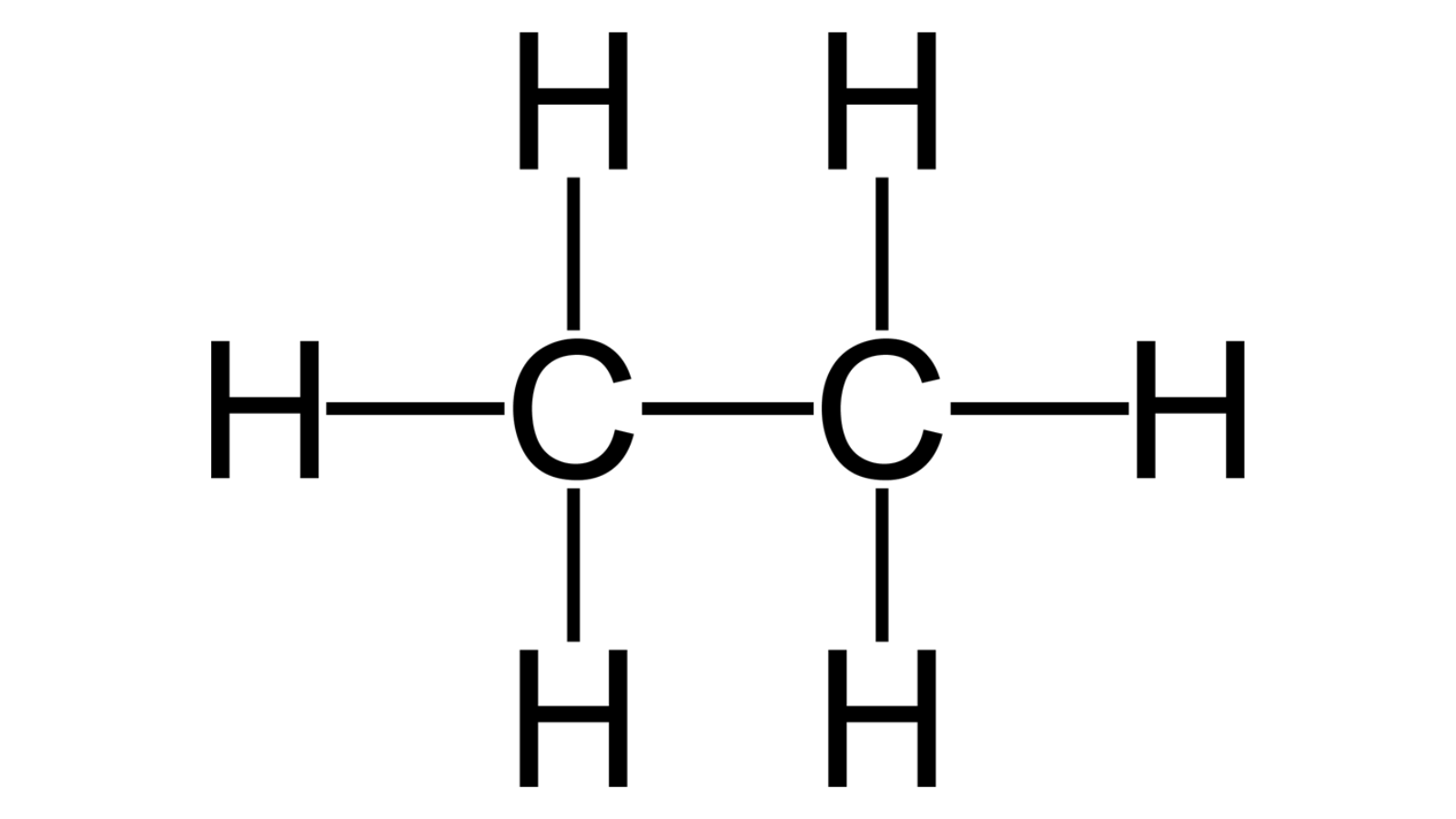
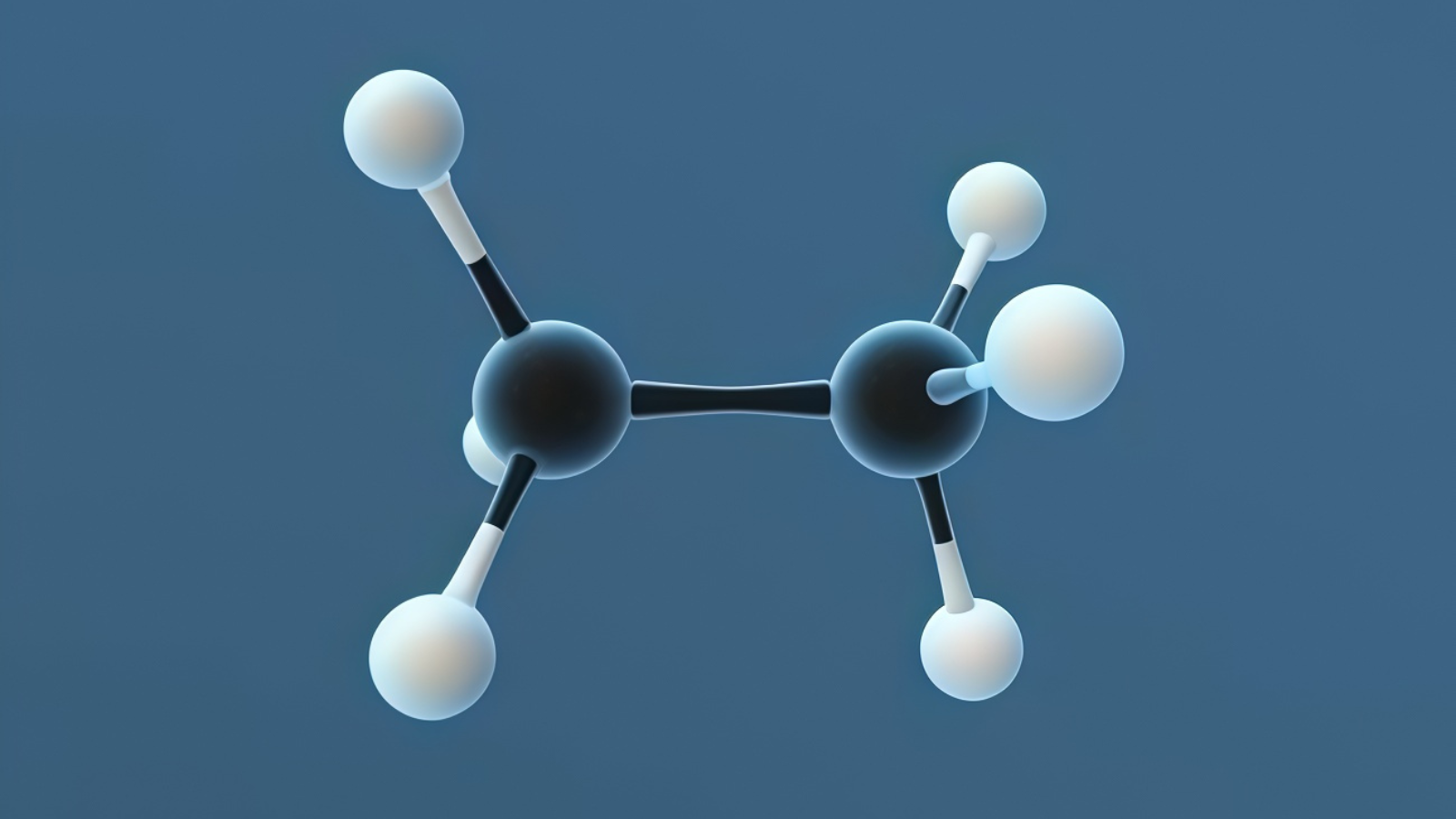
Trong hóa học hữu cơ, ankan là hydrocacbon bão hòa, mạch hở. Điều này có nghĩa là:
- Hydrocarbon: Phân tử chỉ được tạo thành từ hai nguyên tố: Carbon (C) và Hydrogen (H).
- Không: Phân tử chỉ chứa các liên kết đơn ổn định (liên kết sigma σ), không có liên kết đôi hoặc ba.
- Chuỗi mở: Các nguyên tử carbon liên kết với nhau tạo thành chuỗi thẳng hoặc phân nhánh chứ không khép kín thành vòng.
Tất cả các ankan đều có cùng công thức chung CnH2n+2 (với điều kiện n ≥1). Trong đó ‘n’ là số lượng nguyên tử Carbon. Các hợp chất có cùng công thức chung và tính chất hóa học tương tự như Ankan được xếp vào cùng một dãy đồng đẳng.
Ankan còn có một tên cũ khá phổ biến là Paraffin, bắt nguồn từ tiếng Latin parum affiniscó nghĩa là “ít ái lực hóa học”. Tên gọi này bắt nguồn từ việc ankan khá trơ về mặt hóa học, chúng khó tham gia phản ứng trong điều kiện bình thường vì chỉ chứa các liên kết đơn rất bền.
2. Cách gọi tên các Ankan (Danh pháp IUPAC) và các gốc Alkyl thông dụng
Gọi đúng tên một hợp chất hữu cơ là một kỹ năng cơ bản và cực kỳ quan trọng. Đối với Alkanes, chúng tôi tuân theo các quy tắc của Liên minh Hóa học thuần túy và ứng dụng quốc tế (IUPAC).
Bảng tên 10 ankan đầu tiên và các gốc ankyl tương ứng
Để đặt tên cho Alkanes, chúng ta sử dụng tiền tố chỉ lượng Carbon và kết hợp với hậu tố “-an”. Gốc alkyl tương ứng được tạo ra bằng cách thay thế đuôi “-an” bằng đuôi “-yl”. Dưới đây là bảng tham khảo nhanh cần ghi nhớ:
|
Số C (n) |
Công thức phân tử (CnH2n+2) |
Tên ankan |
Công thức gốc (CnH2n+1) |
Tên gốc Alkyl |
|
1 |
CH4 |
Mêtan |
−CH3 |
Metyl |
|
2 |
C2H6 |
Ethan |
−C2H5 |
Etyl |
|
3 |
C3H8 |
Propane |
−C3H7 |
Propyl |
|
4 |
C4H10 |
Butan |
−C4H9 |
Butyl |
|
5 |
C5H12 |
Ngũ Cung |
−C5H11 |
pentyl |
|
6 |
C6H14 |
Hexan |
−C6H13 |
Hexyl |
|
7 |
C7H16 |
Heptan |
−C7H15 |
Heptyl |
|
8 |
C8H18 |
Octane |
−C8H17 |
Octyl |
|
9 |
C9H20 |
Nonan |
−C9H19 |
Nonyl |
|
10 |
C10H22 |
decan |
−C10H21 |
Decyl |
Hướng dẫn 4 bước đặt tên ankan mạch nhánh
Với các Alkan phân nhánh phức tạp hơn, chúng ta thực hiện theo 4 bước sau:
- Chọn mạch chính: Mạch cacbon dài nhất và có nhiều nhánh nhất.
- Đánh số: Bắt đầu đánh số từ đầu mạch gần nhánh hơn, sao cho tổng số chỉ vị trí các nhánh là nhỏ nhất.
- Đặt tên cho chi nhánh: Tên chi nhánh bao gồm: [Số chỉ vị trí nhánh]-[Tên gốc Ankyl]. Nếu có nhiều nhánh giống nhau thì thêm các tiền tố di- (2), tri- (3), tetra- (4)…
- Ghép nối tên đầy đủ: Tên ankan = [Tên nhánh] + [Tên Ankan của mạch chính].
Ví dụ: Gọi tên hợp chất sau:
- Chuỗi chính: Dài nhất là 5 Carbon (Pentane).
- Đánh số: Bắt đầu từ phải sang trái sao cho vị trí nhánh là 2, 2, 4 (tổng là 8), nhỏ hơn chiều từ trái qua phải là 2, 4, 4 (tổng là 10).
- Tên nhánh: Có 3 nhánh Methyl ở vị trí 2, 2, 4. Tên nhánh là: 2,2,4-trimethyl.
- Tên đầy đủ: 2,2,4-trimethylpentane.

Phân biệt Akan và Aken bằng thuốc tím
3. Khám phá tính chất hóa học đặc trưng của Ankan
Bởi vì chúng chỉ có các liên kết đơn ổn định nên ankan tương đối trơ về mặt hóa học. Phản ứng của chúng thường đòi hỏi điều kiện khắc nghiệt (nhiệt độ, áp suất, xúc tác). Phản ứng đặc trưng nhất là phản ứng thay thế.
Phản ứng thế halogen – “Dấu ấn” độc đáo của Alkanes
Khi có ánh sáng khuếch tán (as) hoặc nhiệt độ cao, Ankan có thể tham gia phản ứng thế bằng các halogen (thường là Clo, Brom). Trong phản ứng này, nguyên tử Hydro sẽ được thay thế bằng nguyên tử Halogen.
- Nguyên tắc thay thế: Nguyên tử halogen được ưu tiên thay thế nguyên tử Hydro trong Carbon có bậc cao hơn (Cấp III > Cấp II > Cấp I).
Ví dụ: Propane phản ứng với clo theo tỉ lệ mol 1:1.
CH3−CH2−CH3+Cl2asCH3−CH(Cl)−CH3+HCl (Sản phẩm chính, thay thế cho C thứ cấp)
CH3−CH2−CH3+Cl2asCH3−CH2−CH2Cl+HCl (Sản phẩm phụ, thay thế cho C chính)
Phản ứng Cracking và phản ứng dehydro hóa tạo ra sản phẩm gì?
Dưới tác dụng của nhiệt độ cao và chất xúc tác, Ankan có thể bị “phá vỡ” chuỗi Carbon (cracking) hoặc tách khỏi Hydrogen (dehydrogenation) để tạo ra Hydrocarbon có mạch ngắn hơn, thường là Alkan và Alken nhỏ hơn. Đây là một quá trình cực kỳ quan trọng trong ngành lọc dầu để sản xuất xăng và các nguyên liệu thô khác.
- Cracking: CnH2n+2t°,xtCaH2a+2+CbH2b (với a+b = n)
- Khử hydro: CnH2n+2t°,xtCnH2n+H2
Phản ứng đốt cháy của ankan (oxy hóa hoàn toàn)
Tất cả các ankan đều dễ cháy và tỏa ra lượng nhiệt lớn, đó là lý do tại sao chúng được sử dụng làm nhiên liệu. Đốt cháy hoàn toàn trong khí oxi tạo ra khí cacbonic (CO2) và nước (H2O).
Phương trình tổng quát:
CnH2n+2+23n+1O2t°nCO2+(n+1)H2O
Lưu ý: Trong phản ứng đốt ankan, số mol nước (H2O) tạo ra luôn lớn hơn số mol CO2.
Ankan có làm mất màu dung dịch thuốc tím (KMnO4) không?
Câu trả lời là KHÔNG.
Dung dịch kali kali (KMnO4) là chất oxy hóa mạnh và thường được dùng để nhận biết các hợp chất có liên kết đôi hoặc ba (như Anken, Alkynes). Các liên kết này kém bền hơn và dễ bị tấn công bởi các tác nhân oxy hóa. Ngược lại, ankan chỉ chứa liên kết đơn sigma (σ) rất ổn định và không phản ứng với KMnO4 trong điều kiện bình thường. Đây là một trong những cách phổ biến nhất để phân biệt ankan với các hydrocacbon không bão hòa khác.
4. Tính chất vật lý và ứng dụng của Ankan trong đời sống và công nghiệp
Tính chất vật lý của ankan thay đổi đều đặn khi số lượng nguyên tử cacbon tăng lên.
|
đặc trưng |
Xu hướng thay đổi khi chuỗi Carbon tăng |
|
Trạng thái |
C1−C4: Khí. C5−C17: Chất lỏng. ≥C18: Chất rắn (sáp parafin). |
|
Nhiệt độ sôi, nhiệt độ nóng chảy |
Tăng dần. Các ankan phân nhánh thường có nhiệt độ sôi thấp hơn các đồng phân mạch thẳng. |
|
độ hòa tan |
Hầu như không tan trong nước (do là hợp chất không phân cực), nhưng tan trong dung môi hữu cơ không phân cực. |
|
khối lượng cụ thể |
Nhẹ hơn nước (D<1g/cm3). |
Nhờ tính chất đa dạng, Alkanes có vô số ứng dụng quan trọng:
- Nhiên liệu: Metan trong khí tự nhiên, Propane và Butane trong khí dầu mỏ hóa lỏng (LPG), ankan lỏng là thành phần chính của xăng, dầu hỏa và diesel.
- Dung môi: Các ankan lỏng như Hexane và Heptane được sử dụng làm dung môi để hòa tan chất béo và dầu.
- Chất bôi trơn: Các ankan có trọng lượng phân tử lớn được dùng làm chất bôi trơn để bôi trơn máy móc.
- Nguyên liệu sản xuất: Từ Alkan người ta có thể điều chế được Alken, Hydro và nhiều dẫn xuất Halogen, làm tiền đề cho các ngành công nghiệp polyme, nhựa và các ngành hóa chất khác.
- Sáp parafin: Dùng làm nến, giấy sáp, chống thấm, mỹ phẩm…

Ứng dụng của Ankan trong đời sống
5. Bài tập Alkane nâng cao và cơ bản (có giải thích chi tiết)
Loại 1: Sự cố cháy
Đốt cháy hoàn toàn 4,48 lít khí Butan (C4H10) ở điều kiện thường. Tính thể tích khí oxi cần dùng và thể tích nước thu được.
- Giải:Số mol Butan: nC4H10=22,44,48=0.2 (mol) Phương trình phản ứng: C4H10+213O2t°4CO2+5H2OATheo PTHH:nO2=213×nC4H10=213×0.2=1.3 (mol)⟹VO2=1,3×22,4=29,12 (lít)nH2O=5×nC4H10=5×0,2=1 (mol)⟹mH2O=1×18=18 (gram)
Loại 2: Vấn đề phản ứng thay thế
Cho 11,6 gam Butan phản ứng với Clo (thắp sáng) theo tỷ lệ mol 1:1. Tính khối lượng sản phẩm hữu cơ chính thu được.
- Lời giải:MC4H10=58 g/mol. nC4H10=5811.6=0.2 (mol)Butan có công thức: CH3−CH2−CH2−CH3. Carbon thứ cấp ở vị trí 2 và 3 là vị trí ưa thích. PTHH: CH3−CH2−CH2−CH3+Cl2asCH3−CH(Cl)−CH2−CH3+HClSản phẩm chính là 2-chlorobutane (C4H9Cl).Theo PTHH, nC4H9Cl=nC4H10=0.2 (mol).MC4H9Cl=12×4+9+35,5=92,5 g/mol.Khối lượng sản phẩm chính: m=0,2×92,5=18,5 (gram).
Dạng 3: Tìm công thức phân tử của Ankan
Đốt cháy hoàn toàn một ankan X thu được 17,6 gam CO2 và 9 gam H2O. Tìm CTPT của X.
- Giải pháp:nCO2=4417.6=0.4 (mol)nH2O=189=0.5 (mol) Vì nH2O>nCO2, X là Ankan. Gọi CTPT của X CnH2n+2. Ta có tỉ số: n+1n=nH2OnCO2=0.50,4=54⟹5n=4(n+1)⟹5n=4n+4⟹n=4Vậy CTPT của X là C4H10.
6. Câu hỏi thường gặp – Giải đáp nhanh các câu hỏi thường gặp về Alkanes
- Alkanes và Paraffin có giống nhau không?
Đúng, “Paraffin” là tên cũ của Alkane. Cả hai đều đề cập đến các hydrocacbon bão hòa, không vòng có công thức chung CnH2n+2.
- Thứ tự cacbon trong ankan như thế nào?
Mức độ của một nguyên tử Carbon được tính bằng số lượng nguyên tử Carbon khác liên kết trực tiếp với nó. Có 4 cấp độ: Cấp I, II, III và IV.
- Đồng phân của ankan là gì? Cho ví dụ về đồng phân của C4H10.
Đồng phân là những hợp chất khác nhau nhưng có cùng công thức phân tử. Từ C4 trở đi, ankan có đồng phân mạch cacbon.
C4H10 có 2 đồng phân:
- Butan (chuỗi thẳng): CH3−CH2−CH2−CH3
- Isobutane (2-methylpropane, chuỗi phân nhánh): CH3−CH(CH3)−CH3
Bài viết này được chỉnh sửa bởi SĐược biên soạn bởi đội ngũ chuyên gia hóa học của Trường Chu Văn An và có sự tư vấn từ các tài liệu Hóa học chuyên ngành, đảm bảo tính chính xác và cập nhật.
Nguồn tham khảo:
- Sách giáo khoa Hóa lớp 11, Nhà xuất bản Giáo dục Việt Nam.
- IUPAC. Bản tóm tắt thuật ngữ hóa học, tái bản lần thứ 2. (“Sách vàng”). (1997).
- Morrison, RT, & Boyd, RN (1992). Hóa hữu cơ (tái bản lần thứ 6). Prentice-Hall.


Nội dung được phát triển bởi đội ngũ truongchuvananhue.edu.vn với mục đích chia sẻ và tăng trải nghiệm khách hàng. Mọi ý kiến đóng góp xin vui lòng liên hệ tổng đài chăm sóc: 1900 0000 hoặc email: hotro@truongchuvananhue.edu.vn